题目内容
【题目】某兴趣小组利用下列装置,进行与氯气相关的实验。
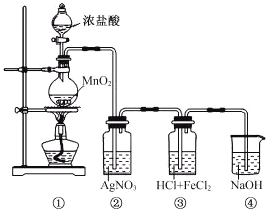
(1)装置④中NaOH溶液的作用是___________。
(2)实验结束后,取装置③中的溶液,经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到FeCl3·6H2O晶体。在蒸发浓缩操作中,不需要的仪器是___________。
A.蒸发皿 B.漏斗 C.玻璃棒 D.酒精灯
(3)装置②中出现白色沉淀,据此现象能否推测装置①中生成Cl2___________________,请说明理由_______________________________________。
【答案】吸收氯气 B 否 浓盐酸挥发出的氯化氢也能与硝酸银反应,也能出现白色沉淀
【解析】
装置①为氯气制备装置,装置②中氯气和挥发出的氯化氢能与硝酸银反应生成白色沉淀,装置③氯气能够将氯化亚铁氧化生成氯化铁,装置④中氢氧化钠溶液吸收有毒的氯气,防止污染环境。
(1)装置④中NaOH溶液的作用是吸收有毒的氯气,防止污染环境,故答案为:吸收氯气;
(2)在蒸发浓缩操作中,需要用到的仪器有蒸发皿、三脚架、玻璃棒、酒精灯,不需要漏斗,故答案为:B;
(3)氯气与水反应生成盐酸和次氯酸,盐酸与硝酸银反应,生成氯化银白色沉淀,由于盐酸具有挥发性,氯气中混有的挥发出的氯化氢也能与硝酸银反应,生成氯化银白色沉淀,因此不能依据装置②中出现白色沉淀推测装置①中生成Cl2,故答案为:否;浓盐酸挥发出的氯化氢也能与硝酸银反应,也能出现白色沉淀。

 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案【题目】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请选择适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。

(1)A是制取CO2的装置.写出A中发生反应的化学方程式___________________。
(2)填写表中空格:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | 除去二氧化碳中的氯化氢 |
C | ____________ | ____________ |
D | NaOH溶液 | ____________ |
(3)写出C中发生反应的化学方程式:___________________。
(4)试管F中收集满气体后,下一步实验操作是把E中的导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管,立即把_____________________,则证明试管中收集的气体是氧气。