题目内容
18. 钠、铁和铝是三种重要的金属.请回答:
钠、铁和铝是三种重要的金属.请回答:(1)三种金属的金属性由强到弱的顺序是:Na>Al>Fe.
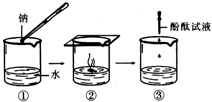
(2)钠跟水反应的过程如图所示,试写出该反应的化学方程式2Na+2H2O=2NaOH+H2↑;
③中加入酚酞试液后观察到的现象是溶液变红色.
(3)常温下,铁、铝两种金属中,能与氢氧化钠溶液发生反应的是Al(或铝),写出该反应的化学方程式:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(4)将氢氧化钠溶液滴入氯化铁溶液中,发生反应的离子方程式为Fe3++3OH-=Fe(OH)3↓;
在氯化铝溶液中逐滴滴入过量的氢氧化钠溶液,观察到的现象是b(填序号).
a.只放出气体
b.产生白色沉淀,随后沉淀溶解
c.只产生白色沉淀
d.既产生白色沉淀,又放出白色气体.
分析 (1)利用金属活动性顺序表,结合其排在前面的金属的活动性大于后面的金属的意义判断金属活动性强弱;
(2)钠和水反应生成氢氧化钠和氢气;酚酞遇碱变红;
(3)铁和氢氧化钠不反应,铝能和强酸、强碱反应,金属铝与氢氧化钠溶液反应生成了偏铝酸钠和氢气;
(4)FeCl3和NaOH反应生成红褐色沉淀Fe(OH)3;AlCl3中加入NaOH先生成Al(OH)3,Al(OH)3具有两性,可与NaOH反应生成NaAlO2,以此解答.
解答 解:(1)金属活动性顺序是:K、Ca、Na、Mg、Al、Mn、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au,结合活动性前大于后;则钠、铁和铝三种金属活动性由强到弱的顺序是Na、Al、Fe,
故答案为:Na>Al>Fe;
(2)钠是一种非常活泼的金属,将其投入水中,会浮在水面上与水发生剧烈反应,放出的热使其熔化成银白色小球,甚至使生成的氢气燃烧,发生反应的化学方程式为:2Na+2H2O═2NaOH+H2↑,酚酞遇碱变红,③中加入酚酞试液后观察到的现象是溶液变红色,
故答案为:2Na+2H2O═2NaOH+H2↑;溶液变红色;
(3)铝和强酸、强碱反应生成可溶性盐和氢气;铝与氢氧化钠溶液反应,反应生成偏铝酸钠和氢气,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:Al(或铝);2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(4)FeCl3和NaOH反应生成红褐色沉淀Fe(OH)3,化学方程式为FeCl3+3NaOH=Fe(OH)3↓+3NaCl,离子方程式为 Fe3++3OH-=Fe(OH)3↓,AlCl3中加入NaOH先生成白色沉淀Al(OH)3,发生Al3++3OH-═Al(OH)3↓,Al(OH)3具有两性,继续加入NaOH溶液则发生Al(OH)3+OH-═AlO2-+2H2O,可观察到沉淀溶解,
故答案为:Fe3++3OH-=Fe(OH)3↓;b.
点评 本题考查金属活动性的比较、钠与水的反应、铝的化合物的性质等知识,注意金属性的比较,需明确常见的金属性比较的方法,掌握AlCl3中加入NaOH的反应原理是解答的关键,题目难度中等.

 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案| A. | 0.5 mol CO+1.5 mol H2O(g)+0.4 mol CO2+0.4 mol H2 | |
| B. | 0.5 mol CO+2 mol H2O(g)+1 mol CO2+1 mol H2 | |
| C. | 0.5 mol CO+1.5 mol H2O(g)+0.5 mol CO2+0.5 mol H2 | |
| D. | 1 mol CO+1 mol H2O(g)+1 mol CO2+1 mol H2 |
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
| A. | 利用铝热剂的反应,常用于冶炼高熔点的金属 | |
| B. | 氧化铝和铁的混合物是铝热剂 | |
| C. | 铝热剂发生的铝热反应需要用镁带和氯酸钾引燃,所以铝热反应是吸热反应 | |
| D. | 工业上常用铝热反应来大量冶炼金属铁 |
| A. | 不可以用铜丝搅拌棒代替环形玻璃搅拌棒 | |
| B. | 用稍过量的NaOH溶液保证盐酸完全被中和 | |
| C. | 使用环形玻璃搅拌棒是为了加快反应速率,减小实验误差 | |
| D. | 用0.5 mol•L-1NaOH溶液分别与0.5 mol•L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 |
| A. | 聚氯乙烯 | B. | 聚苯乙烯 | C. | 聚四氟乙烯 | D. | 有机玻璃 |
