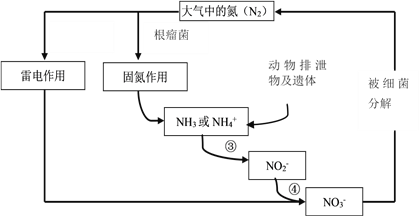
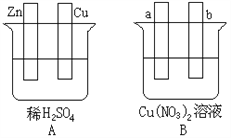
��Ŀ����
����Ŀ��SCR��������Ч���Ͳ��ͷ�����β����NOx���ŷš�SCR��ѡ���Դ���ԭ������ԭ����ͼ��ʾ��

��1������β��ֱ���ŷŻ����_______
a. ���������� b. ���������� c. ������ն�
��2������[CO(NH2)2]ˮ��Һ�ȷֽ�ΪNH3��CO2����Ӧ����NH3���Ի�ԭNO2����ת���к�����Ϊ�����ʵ����ã���֪�μӷ�Ӧ�İ�����NO2�������Ϊ��:�����䷴Ӧ����ʽΪ_________��
��3������Ԫ���غ㣬���մ����������N2��H2O������_______��
��4����ͨ��β���к�67.2L NO2����״���������백����ȫ��Ӧת�Ƶ�����Ϊ_____mol��
���𰸡� a ��acҲ���֣� 8NH3+6NO2==7N2+12H2O CO2 12
����������1��a������β���е���������ֱ���ŷŻ�������е�������ˮ������������������������꣬��a��ȷ��b������β���к������ʺ��٣��ʲ����γ����������꣬��b����c������������ֱ���ŷŵ������У�Ҳ��Գ���������ƻ����ã���c��ȷ����ѡa��ac����2��������NO2�������Ϊ��:�����䷴Ӧ����ʽΪ8NH3+6NO2==7N2+12H2O����3������Ԫ���غ㣬������C��H��O�Ϳ����е������մ����������N2��H2O������CO2����4����ͨ��β���к�67.2L NO2����״������n( NO2)=67.2L/22.4L��mol��1=3mol����8NH3+6NO2==7N2+12H2O��ÿ6molNO2��Ӧת��24mol��������3molNO2�백����ȫ��Ӧת�Ƶ�����Ϊ12mol��

 ��������������������ϵ�д�
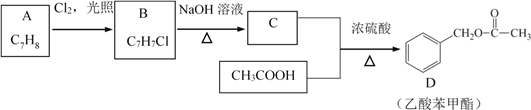
��������������������ϵ�д�����Ŀ����Ȼ���е����ʾ�������Ի�������ʽ���ڣ�Ϊ�˱����о������ã�����Ի������з�����ᴿ������A��B��C��D����ѧ�����Ļ���������ᴿ��װ�á�
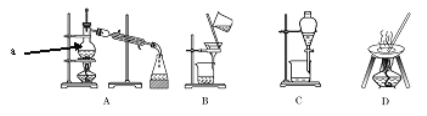
��������ݻ���������ᴿ��ԭ�����ش�������ʵ������Ҫʹ������װ�á���A��B��C��D�����ʵ��Ŀո��С�
��1��̼�������Һ�з����̼���___________��
��2���Ȼ�����Һ�з�����Ȼ���___________��
��3������ֲ���ͺ�ˮ___________��
��4����ˮ����___________��
��5���Ȼ�����Һ�з����ˮ___________��
��6����ȥ����ˮ�е�Cl��������___________��
��7���ӵ�ˮ�з����I2___________��
������ˮ����ȡ�ⵥ�ʵķ������£�
��1����ȡ��Һ
�����п���Ϊ��ˮ����ȡ�ⵥ����ȡ������___________��
A���ƾ� B����
�ڷ�Һ©����ʹ��ǰ������___________��
�۲����ϵ�֪���ѣ�H2O��>��������>�����ƾ��������â�����ѡ��ȡ����ȡ��ˮ�еĵⵥ�ʣ���Һʱ��ˮ��Ӧ�ɷ�Һ©����______�˿ڷų����л���Ӧ�ɷ�Һ©����______�˿ڷų���������������������������
��2������
��װ��A��a��������_______������װ��������ˮӦ��________�ڽ�������������������������������Ŀ����________________________��װ��C�ڷ�ҺʱΪʹҺ��˳�����£�����©���¶˵������⣬��Ӧ���еľ��������__________________________��
����֪������Ȼ�̼���۷е��������±�
�۵� | �е� | |
�� | 113.7�� | 184.3�� |
���Ȼ�̼ | -22.6�� | 76.8�� |
���������������Ȼ�̼�Ļ�����ƿ�����ռ��������ʵ�������___________��
��. ��ˮ���̲��ŷḻ����Դ����ʵ������ȡ������ˮ�������������̵�ʵ�飺

����һ�������к�Ca2+��Mg2+��SO42�������ʣ���Ҫ�ᴿ������ۺ����á������ᴿ�IJ����У�
�ټ��������Na2CO3��Һ���ڼ��������BaCl2��Һ���ۼ��������NaOH��Һ���ܵ�����Һ��pH����7�����ܽ� ���ˡ���������ȷ�IJ���˳����__________����ѡ����ĸ��.
�ݢڢۢ٢ޢܢ� b���ݢ٢ڢۢޢܢ� c���ݢڢ٢ۢܢޢ� d���ݢۢڢ٢ޢܢ�
��������ɺ�ˮ���Ȼ��ƾ����ʵ�������Ҫ�õ�����Ҫװ����_________________���Ӹ���������װ����ѡ������ĸ����
�������������к���������ɳ��CaCl2��MgCl2�������Σ��������ܽ���ȹ��˽���ɳ��ȥ���ټ�����Һ�е�SO42����������Һ�е�SO42����ʵ�������������_________________________��