题目内容
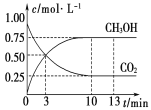
【题目】已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。一定条件下,向体积为1 L的恒容密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中正确的是 ( )
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。一定条件下,向体积为1 L的恒容密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中正确的是 ( )
A. 3min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率
B. 从反应开始到平衡,H2的平均反应速率v(H2)=0.225 mol·L-1·min-1
C. 13min时,向容器中充入2 mol氦气,该反应的化学反应速率增加
D. 13min时,向容器中充入2 mol氦气,CO2的转化率增加
【答案】B
【解析】
试题A.3 min时,CH3OH和CO2的浓度相等,但是并没有达到平衡,用CO2的浓度表示的正反应速率与用CH3OH的浓度表示的逆反应速率不相等,故A错误;B.根据图像可知,10min时达到化学平衡,则从反应开始到平衡,二氧化碳的平均反应速率="=0.075" mol·L-1·min-1,根据反应速率之比等于方程式中化学计量数之比,则H2的平均反应速率0.225mol·L-1·min-1,故B正确;C.13min时,向容器中充入2mol氦气,因体积不变,则各组分浓度不变,该反应的化学反应速率不变,平衡不发生移动,CO2的转化率不变,故C错误;D.向容器中充入2mol氦气,该反应的化学反应速率不变,平衡不发生移动,CO2的转化率不变,故D错误;

练习册系列答案
相关题目