题目内容
【题目】常温下,等体积的氨水和KOH两种溶液,其![]() ,下列说法正确的是
,下列说法正确的是![]()
A.![]() 的浓度小于KOH
的浓度小于KOH
B.分别向两溶液中加入盐酸完全中和后,溶液中水的电离程度前者大于后者
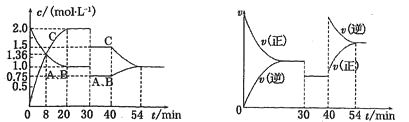
C.两溶液加水稀释过程中 、
、 均增大
均增大
D.分别加水稀释相同倍数后,溶液中![]()
【答案】B
【解析】
A、![]() 是弱碱部分电离,而KOH为强碱完全电离;
是弱碱部分电离,而KOH为强碱完全电离;
B、分别向两溶液中加入盐酸完全中和后,前者生成氯化铵和后者生成氯化钾;
C、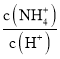 的分子和分母都乘氢氧根离子的浓度,得到
的分子和分母都乘氢氧根离子的浓度,得到![]() ,由此分析解答;
,由此分析解答;
D、加水稀释钾离子和铵根离子的浓度都减小,但加水稀释加水稀释促进一水合氨的电离,所以铵根离子浓度变大。
![]() 是弱碱部分电离,而KOH为强碱完全电离,而等体积的氨水和KOH两种溶液,其
是弱碱部分电离,而KOH为强碱完全电离,而等体积的氨水和KOH两种溶液,其![]() ,所以
,所以![]() 的浓度大于KOH,故A错误;
的浓度大于KOH,故A错误;
B、分别向两溶液中加入盐酸完全中和后,前者生成氯化铵和后者生成氯化钾,氯化铵溶液水解呈酸性,对水的电离起促进作用,所以溶液中水的电离程度前者大于后者,故B正确;
C、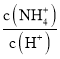 的分子和分母都乘氢氧根离子的浓度,得到
的分子和分母都乘氢氧根离子的浓度,得到![]() ,加水稀释过程一水合氨的浓度减小,比值减小,故C错误;
,加水稀释过程一水合氨的浓度减小,比值减小,故C错误;
D、加水稀释钾离子和铵根离子的浓度都减小,但加水稀释促进一水合氨的电离,所以铵根离子浓度变大,即溶液中![]() ,故D错误;
,故D错误;
故选:B。

【题目】乙醛在氧化铜作催化剂的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示,试管A中装有40%的乙醛水溶液、氧化铜粉末;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见表:
物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
沸点(℃) | 20.8 | 117.9 | 290 | 197.2 | 100 |

请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为_______________。
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在试管A的反应液中;目的是___________;当试管A内的主要反应完成后温度计水银球的位置应在试管A的支管口处;目的是_________。
(3)烧杯B的作用是使试管A内的反应液均匀受热发生反应,使生成的乙酸变成蒸气进入试管C,烧杯B内盛装的液体可以是____。(写出一种即可,在题给物质中找);某同学认为试管C最好置于冰水浴中,其目的是________。
(4)对C中产品进行蒸馏时,蒸馏烧瓶中加入少量___,以除去其中含有的少量水。
A.浓硫酸 B.CaO C.CuSO4溶液 D.无水CaCl2
(5)以下区分乙酸精品和粗品的方法,合理的是_____。
A.加入水观察实验现象
B.加入足量氢氧化钠溶液后,再加入银氨溶液,水浴加热观察实验现象
C.加入碳酸氢钠溶液,振荡后观察实验现象
D.加入少量Na单质,振荡后观察实验现象