题目内容
W、X、Y、Z是元素周期表中前四周期元素,它们在周期表中的相对位置如图所示。
下列有关叙述中正确的是

A.Z元素一定是金属元素
B.X、Y、W一定是主族元素
C.若W的单质在空气中燃烧有三种固体产物,则Y的单质既能与强酸溶液反应又能与强碱溶液反应
D.Z既可能在三周期,也可能在四周期
B
【解析】根据周期表的结构可知,选项A是错误的,Z也可能是非金属。X、Y、W一定位于短周期,所以一定是主族元素,B正确。单质既能与强酸溶液反应又能与强碱溶液反应是铝,根据周期表的结构,铝和镁是不相邻的,C不正确。Z只能是第四周期元素,D不正确 ,答案选B。

 一课一练课时达标系列答案
一课一练课时达标系列答案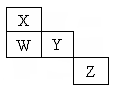 如图为元素周期表前四周期的一部分,W、X、Y、Z是元素周期表中前四周期元素,它们在周期表中的相对位置如表中所示.下列有关叙述中正确的是( )
如图为元素周期表前四周期的一部分,W、X、Y、Z是元素周期表中前四周期元素,它们在周期表中的相对位置如表中所示.下列有关叙述中正确的是( )| A、Z元素一定是金属元素 | B、X、Y、W一定是主族元素 | C、W的氢化物的沸点一定比X的氢化物的沸点高 | D、Z既可能在三周期,也可能在四周期 |
W、X、Y、Z是元素周期表中原子前四周期的四种元素,有关它们的信息如下表所示。
元素 | 相关信息 |
W | W的基态原子L层电子数是K层电子数的3倍 |
X | X与氢元素形成的一种化合物可以使湿润的红色石蕊试纸变蓝 |
Y | 单质为黄绿色气体,最高价氧化物对应的水化物化学式为HYO4 |
Z | Z的基态原子外围电子排布式为(n-1)d10ns1 |
(1)Y位于元素周期表第________周期第________族;X的基态原子核外电子排布式是??????????? 。
(2)W的简单离子半径???? X的简单离子半径(填“>”、“<”或“=”);Y的第一电离能比Z的???? (填“大”或“小”);W、X的最简单气态氢化物中,沸点较高的是??????? (填化学式)。
(3)在150℃左右时,化合物ZW与氢气反应生成红色的Z2W粉末,该反应的化学方程式为??????? 。
(4)W元素形成的多种化合物分子中,含有极性共价键和非极性共价键的分子名称为
???????????????????????? (任写一种)。
(5)在25℃、101 kPa下,已知Z固体单质在Y2气体中完全燃烧后恢复至原状态,平均每转移1mol 电子放热110.05kJ,该反应的热化学方程式是?????? ? ???? ???????????????????????????????? 。