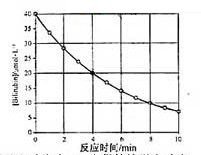
题目内容
反应E+F=G在温度t1下进行 ,反应M+N=K在温度t2下进行,已知t1>t2,且E和F的浓度均大于M和N的浓度(其他条件均相同),则两者
,反应M+N=K在温度t2下进行,已知t1>t2,且E和F的浓度均大于M和N的浓度(其他条件均相同),则两者 的反应速率
的反应速率
 ,反应M+N=K在温度t2下进行,已知t1>t2,且E和F的浓度均大于M和N的浓度(其他条件均相同),则两者
,反应M+N=K在温度t2下进行,已知t1>t2,且E和F的浓度均大于M和N的浓度(其他条件均相同),则两者 的反应速率
的反应速率| A.前者大 | B.后者大 | C.相等 | D.无法判断 |
D
略

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 速率最大的是
速率最大的是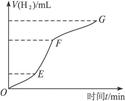
 2NH3的反应中,各物质的起始浓度分别为:c(H2)="4" mol·L-1,c(N2)="3" mol·L-1,c(NH3)="0.5" mol·L-1,经3 min后,c(NH3)="0.8" mol·L-1,该反应的反应速率是( )
2NH3的反应中,各物质的起始浓度分别为:c(H2)="4" mol·L-1,c(N2)="3" mol·L-1,c(NH3)="0.5" mol·L-1,经3 min后,c(NH3)="0.8" mol·L-1,该反应的反应速率是( ) 2AB2(g); 正反应为放热反应,下列说法正确的
2AB2(g); 正反应为放热反应,下列说法正确的