题目内容
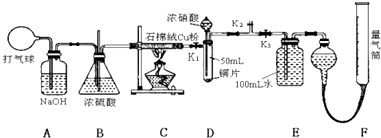
12.下列装置能达到相应实验目的是( )| A. | 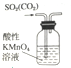 装置,除去SO2中混有的CO2 | |
| B. |  装置,用于亚硫酸钠和硫酸反应制取少量的SO2 | |
| C. | 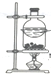 装置,分离NH4Cl和Ca(OH)2固体 | |
| D. | 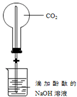 装置,做喷泉实验 |
分析 A.二氧化硫与高锰酸钾发生氧化还原反应;
B.亚硫酸钠为粉末固体,反应后关闭止水夹不能使固体与液体分离;
C.NH4Cl和Ca(OH)2固体加热发生反应;
D.二氧化碳与NaOH溶液反应,导致产生压强差,可形成喷泉.
解答 解:A.二氧化硫与高锰酸钾发生氧化还原反应,将原物质除去,不能除杂,应选饱和碳酸氢钠、洗气,故A错误;
B.亚硫酸钠为粉末固体,反应后关闭止水夹不能使固体与液体分离,则不能利用简易装置制备少量气体,故B错误;
C.NH4Cl和Ca(OH)2固体加热发生反应,则升华装置不能分离,故C错误;
D.二氧化碳与NaOH溶液反应,导致产生压强差,可形成喷泉,则图中装置可完成喷泉实验,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、气体的制备、喷泉实验等,把握物质的性质、反应原理为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
2.某化学反应 3A(g)?2B(g)+D(g),在四种不同条件下进行,B、D的起始浓度为0.反应物A 的浓度 c 随时间 t 的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验 1,反应在10min~20min 内平均速率v(A)为0.03 mol/(L•min)
(2)在实验 2,A 的初始浓度 C22.0 mol/L,反应经 20min 就达到平衡,可推测实验 2 中还隐含的条件是使用催化剂.
(3)设实验 3 的反应速率为 v3,实验 1 的反应速率为 v1,则 v3>v1(填<、>或=),且C3> 2.0mol/L (填<、>或=)
(4)比较实验 4 和实验 1,可推测正反应是放热反应(填吸热或放热).理由是温度升高,A的浓度增大,平衡向吸热方向移动
(5)该反应化学平衡常数表达式为$\frac{{c}^{2}(B)×c(D)}{{c}^{3}(A)}$.
| 实验序号 |  | 0 | 10 | 20 | 30 | 40 | 50 |
| 1 | 500 | 2.0 | 1.6 | 1.3 | 1.0 | 0.8 | 0.8 |
| 2 | 500 | C2 | 1.2 | 0.8 | 0.8 | 0.8 | 0.8 |
| 3 | 500 | C3 | 1.7 | 1.3 | 1.0 | 1.0 | 1.0 |
| 4 | 600 | 2.0 | 1.1 | 0.9 | 0.9 | 0.9 | 0.9 |
(1)在实验 1,反应在10min~20min 内平均速率v(A)为0.03 mol/(L•min)
(2)在实验 2,A 的初始浓度 C22.0 mol/L,反应经 20min 就达到平衡,可推测实验 2 中还隐含的条件是使用催化剂.
(3)设实验 3 的反应速率为 v3,实验 1 的反应速率为 v1,则 v3>v1(填<、>或=),且C3> 2.0mol/L (填<、>或=)
(4)比较实验 4 和实验 1,可推测正反应是放热反应(填吸热或放热).理由是温度升高,A的浓度增大,平衡向吸热方向移动
(5)该反应化学平衡常数表达式为$\frac{{c}^{2}(B)×c(D)}{{c}^{3}(A)}$.
3.下列化学用语的表达或使用正确的是( )
| A. | 白磷的分子式:P | B. | 次氯酸的结构式:H-Cl-O | ||
| C. | 氟离子的结构示意图: | D. | 过氧化氢的电子式: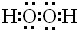 |
20.用10mL的0.1mol•L-1 BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是( )
| A. | 3:2:2 | B. | 1:2:3 | C. | 1:3:3 | D. | 3:1:1 |
7.下列化学用语表达正确的是( )
| A. | CO2分子比例模型: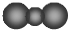 | |
| B. | 氨基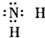 | |
| C. | 原子结构示意图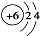 表示12C,也可以表示14C 表示12C,也可以表示14C | |
| D. | 乙炔的最简式 CH≡CH |
1.对已达化学平衡的下列反应 2X(g)+Y(g)?2Z(g),减小压强时,对反应产生的影响是( )
| A. | 逆反应速率增大,正反应速率减小 | B. | 逆反应速率减小,正反应速率增大 | ||
| C. | 逆反应速率先增大后减小 | D. | 正反应速率先减小后增大 |
2.设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 2.4g镁变为镁离子失去的电子数为0.1NA | |
| B. | 电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g | |
| C. | 标准状况下,2.24L四氯化碳含有分子的数目为0.1NA | |
| D. | 常温常压下,Na2O2与足量H2O反应,当生成0.2molO2时,转移电子的数目为0.4NA |
 .
.