题目内容
【题目】下列说法正确的有几个
①pH=0的溶液中Fe3+与S2因发生双水解而不共存
②MgCl2溶液蒸干后得MgO固体,如果想要得到MgCl2固体应通入HCl的气流
③将0.1mol的Na2CO3溶于水中,形成溶液中阴离子总数小于0.1NA
④已知:AgCl(s)Ag+(aq)+Cl(aq),加少量水稀释平衡右移,c(Ag+)减小.
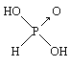
⑤![]() 和
和![]() 在溶液中因为互相抑制水解而大量共存
在溶液中因为互相抑制水解而大量共存
⑥pH=2的盐酸和醋酸,均稀释到pH=5,醋酸加水量大
⑦NaHSO3溶液中加入少量NaOH固体,![]() 将增大
将增大
A.2个B.3个C.4个D.5个
【答案】A
【解析】
①pH=0的溶液中Fe3+与S2-会发生氧化还原反应生成硫沉淀和硫化亚铁沉淀,①错误;
②MgCl2溶液蒸干时氯化镁的水解程度增大,生成氢氧化镁沉淀,氢氧化镁分解得到MgO固体,如果想要得到MgCl2固体应通入HCl的气流,以抑制氯化镁水解,②正确;
③在Na2CO3溶液中存在碳酸钠的水解生成碳酸氢钠和氢氧化钠,阴离子总数增多,③错误;
④已知:AgCl(s)![]() Ag+(aq)+Cl-(aq),加水稀释平衡右移,c(Ag+)浓度不变,④错误;
Ag+(aq)+Cl-(aq),加水稀释平衡右移,c(Ag+)浓度不变,④错误;
⑤![]() 存在电离平衡,电离出的氢离子与
存在电离平衡,电离出的氢离子与![]() 反应生成氢氧化铝沉淀,促进碳酸氢根电离,⑤错误;
反应生成氢氧化铝沉淀,促进碳酸氢根电离,⑤错误;
⑥没有注明盐酸和醋酸溶液的体积相等,无法判断,⑥错误;
⑦NaHSO3溶液中加入少量NaOH固体,促进亚硫酸氢根的电离,![]() 将增大,⑦正确;
将增大,⑦正确;
综上所述,正确的有2个,答案选A。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案【题目】(1)乙醇常被用做饮料的添加剂,在一定的条件下能被氧化为乙醛,乙醇___(“能”或“不能”)使酸性KMnO4溶液褪色;已知常温下,2.3g乙醇和一定量的氧气混合后点燃,恰好完全燃烧,放出68.35kJ热量,则该反应的热化学方程式为___。
(2)已知:
化学键 | Si—Cl | H—H | H—Cl | Si—Si |
键能/kJ·mol-1 | 360 | 436 | 431 | 176 |
且硅晶体中每个硅原子和其他4个硅原子形成4个共价键,工业上制取高纯硅的反应方程式为:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g),该反应的反应热为___kJ·mol-1。
Si(s)+4HCl(g),该反应的反应热为___kJ·mol-1。
(3)已知水的比热容为4.18×10-3kJ·g-1·C-1。10g硫黄在O2中完全燃烧生成气态SO2,放出的热量能使500 g H2O的温度由18℃升至62.4℃,则硫黄的燃烧热为____,热化学方程式为____。