题目内容
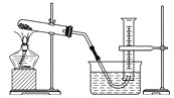
【题目】利用铝热反应焊接钢轨的原理是2Al+Fe2O3![]() 2Fe+Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褐色硬块的组成。
2Fe+Al2O3。某研究小组在实验室利用简易装置进行铝热反应。发现生成的铁呈疏松的褐色硬块。小组成员推测主要原因是产物铁含杂质较多,并进一步探究褐色硬块的组成。
(1)将褐色硬块处理成粉末状。研究小组首先排除了含有单质Al杂质的可能性,实验方法是__,证明不含单质铝的现象是__。
(2)该褐色硬块的组成基本确定为Fe、Fe2O3,Al2O3。请以上述粉末为样品,验证其组成。限选实验仪器与试剂:烧杯、试管、玻璃棒、胶头滴管、药匙、过滤器;20%KSCN、3 mol·L-1NaOH、3mol·L-1HCl、3mol·L-1HNO3、3mol·L-1CuSO4、0.01mol·L-1KMnO4、蒸馏水。
根据你设计的实验方案,叙述实验操作、预期现象和结论。_____。

【答案】取少量粉末加入NaOH溶液中 无气泡冒出 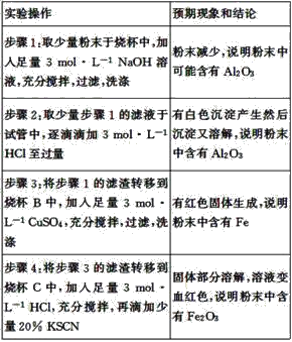
【解析】
(1)根据金属铝可以和氢氧化钠发生反应,而其它物质无此性质;
(2)Fe、Fe2O3、Al2O3中只有氧化铝可以和氢氧化钠发生反应,铁和氧化铁与盐酸发生反应分别生成亚铁盐和铁盐,金属铁可以置换排在金属铁后面的金属,三价铁离子遇到硫氰酸钾显示红色,用此性质逐步验证即可。
(1)根据金属铝可以和氢氧化钠发生反应产生氢气,而其它物质无此性质,若无气体产生则不存在单质铝;
(2)Fe、Fe2O3、Al2O3中只有氧化铝可以和氢氧化钠发生反应,则用3 mol·L-1NaOH浸泡固体物质,向滤液中滴加盐酸,有沉淀出现,后又溶解的现象,则含有Al2O3;铁和氧化铁与盐酸发生反应分别生成亚铁盐和铁盐,金属铁可以置换排在金属铁后面的金属,则取滤渣于试管中,加入足量3mol·L-1CuSO4溶液,若出现红色的固体物质,则含有Fe;三价铁离子遇到硫氰酸钾显示红色,取上述反应后的滤渣,加入足量的3mol·L-1HCl,充分反应后,再加入20%KSCN,若出现红色,则存在氧化铁。

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案【题目】甲醇水蒸气重整制氢方法是目前比较成熟的制氢方法,且具有良好的应用前景。甲醇水蒸气重整制氢的部分反应过程如图所示:
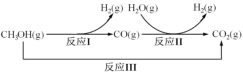
(1)已知一定条件下
反应I:CH3OH(g)=CO(g)+2H2(g) ΔH1=+90.7kJ/mol
反应III:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH3=+49.5kJ/mol
该条件下反应II的热化学方程式是___。
(2)已知反应II在进气比[n(CO):n(H2O)]不同时,在不同温度(T1、T2)下,测得相应的CO的平衡转化率见图。
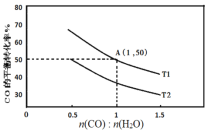
①比较T1、T2的大小,T1___T2(填“>”“<”或“=”)。
②A点对应的化学平衡常数是___。
③T1温度时,按下表数据开始反应建立平衡
CO | H2O | H2 | CO2 | |
起始浓度(mol/L) | 2 | 1 | 0 | 0 |
t时刻浓度(mol/L) | 1.2 | 0.2 | 0.8 | 0.8 |
反应进行到t时刻时,判断v(正)、v(逆)的大小关系为:v(正)___v(逆)(填“>”“<”或“=”)。
④当不同的进气比达到相同的CO平衡转化率时,对应的反应温度和进气比的关系是___。
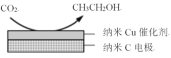
(3)CO2在生产中有着广泛的用途。
①将过量CO2通入KOH溶液中可生成KHCO3,请写出该反应的离子方程式___。
②在经CO2饱和处理的KHCO3弱酸性溶液中,电解活化CO2可以制备乙醇,原理如图所示。该电极为___(填“阴极”或“阳极”),电极反应式是___。