题目内容
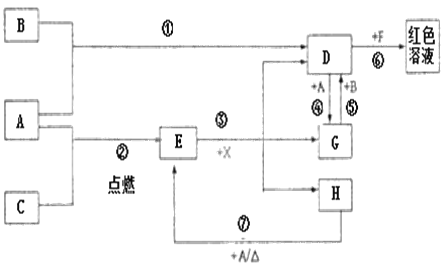
【题目】A、B、C、D为原子序数依次增大的四种短周期元素,已知C、D元素的原子序数之和是A、B元素的原子序数之和的3倍,且C、D元素是同主族元素。甲、乙、丙、丁、戊五种二元化合物的组成如下表:

物质间存在反应:甲+乙→单质B+丙;丁+戊→单质D(淡黄色固体)+丙。下列说法正确的是( )
A.甲、乙、丙、丁、戊均为只含极性键的极性分子
B.原子半径:D>B>C;电负性:B>C>D
C.可用酒精洗涤粘在容器内壁上的单质D
D.若2mol甲与3mol乙恰好反应生成2.5mol单质B,则乙为双原子分子
【答案】D
【解析】
根据单质D为淡黄色固体,则D为S元素;A、B、C、D为原子序数依次增大的四种短周期元素,C、D元素是同主族元素,在C为O元素;C、D元素的原子序数之和是A、B元素的原子序数之和的3倍,A、B元素的原子序数之和为8,戊为O、S两种元素组成的化合物,且丁+戊→单质D(淡黄色固体)+丙,其反应方程式为:2H2S + SO2=3S↓+2H2O、3H2S+SO3=3H2O+4S↓,则A为H元素,B为N元素;甲+乙→单质B+丙,其反应方程式为:8NH3+6NO2=7N2+12H2O、4NH3+6NO=5N2+6H2O,则甲为NH3,乙为NO2或NO,丙为H2O,丁为H2S,戊为SO2或SO3。
A. 若戊为SO3,则SO3是平面正三角形,含极性键的非极性分子,A错误;
B. 同周期,从左到右,原子半径减小,电负性增大;同主族,从上到下,原子半径增大,电负性减小,故原子半径:S>N>O;电负性:O>N>S,B错误;
C. D为S单质,硫微溶于酒精,不能达到洗涤目的,应用二硫化碳洗涤,C错误;
D. 根据4NH3+6NO=5N2+6H2O,若2mol甲与3mol乙恰好反应生成2.5mol单质B,则乙为NO,是双原子分子,D正确;故答案为:D。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
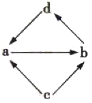
同步拓展阅读系列答案【题目】下表中的各组物质之间通过一步反应就能实现如图所示转化的是( )
编号 | a | b | c | d |
|
① | Na2O | Na2O2 | Na | NaOH | |
② | Al2O3 | NaAlO2 | Al | Al(OH)3 | |
③ | FeCl2 | FeCl3 | Fe | CuCl2 | |
④ | MgO | MgCl2 | Mg | Mg(OH)2 |
A.①②④B.①③④C.①②③D.②③④