题目内容
5.乙醛(CH3CHO)中碳原子的杂化轨道类型为sp3、sp2,1mol乙醛分子中含有的σ键的数目为6NA;乙酸(CH3COOH)的沸点明显高于乙醛,其主要原因是:乙酸的分子间存在氢键,增加了分子之间的作用.分析 乙醛中甲基上的C采取sp3杂化类型,醛基中的C采取sp2杂化类型;1个乙醛分子含有6个σ键和一个π键;乙酸分子间可形成氢键导致沸点较高.
解答 解:乙醛中甲基上的C形成4条σ键,无孤电子对,因此采取sp3杂化类型,醛基中的C形成3条σ键和1条π键,无孤电子对,采取sp2杂化类型;1个乙醛分子含有6个σ键和一个π键,则1mol乙醛含有6molσ键,即6NA个σ键;乙酸分子间可形成氢键,增加了分子之间的作用,乙醛不能形成氢键,所以乙酸的沸点高于乙醛,
故答案为:sp3、sp2;6NA;乙酸的分子间存在氢键,增加了分子之间的作用.
点评 本题考查了氢键、杂化类型、σ键的计算等,题目综合性强,侧重于基础知识的综合应用考查,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.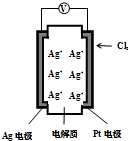 如图所示,利用2Ag+Cl2═2AgCl设计的原电池可测量空气中Cl2的含量(原电池的电解质是含有自由移动Ag+的固体物质).下列分析不正确的是( )
如图所示,利用2Ag+Cl2═2AgCl设计的原电池可测量空气中Cl2的含量(原电池的电解质是含有自由移动Ag+的固体物质).下列分析不正确的是( )
 如图所示,利用2Ag+Cl2═2AgCl设计的原电池可测量空气中Cl2的含量(原电池的电解质是含有自由移动Ag+的固体物质).下列分析不正确的是( )
如图所示,利用2Ag+Cl2═2AgCl设计的原电池可测量空气中Cl2的含量(原电池的电解质是含有自由移动Ag+的固体物质).下列分析不正确的是( )| A. | 空气中c(Cl2)越大,Ag极消耗速率越快 | |
| B. | Ag+向Pt电极移动 | |
| C. | 电子由Ag电极经外电路流向Pt电极 | |
| D. | Ag电极上发生了还原反应 |
16.下列有关电解质溶液的说法正确的是( )
| A. | 在蒸馏水中滴加浓H2SO4,KW不变 | |
| B. | 向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和气体生成 | |
| C. | 中和等体积等物质的量浓度的盐酸和醋酸,所消耗的氢氧化钠的物质的量相同 | |
| D. | NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
13.根据价层电子对互斥理论,判断下列分子或者离子的空间构型不是平面三角形的是( )
| A. | SO3 | B. | BF3 | C. | CO32- | D. | PH3 |
20.下列物质属于电解质的是( )
| A. | 乙醇 | B. | 石墨 | C. | NH3 | D. | 熔融的NaCl |
10.下列气体,可以用排水法收集的是( )
| A. | NO | B. | NH3 | C. | HCl | D. | Cl2 |
17.已知NaBH4中氢元素化合价为-1,反应NaBH4+2H2O═NaBO2+4H2↑中,下列说法正确的是( )
| A. | 被氧化的元素与被还原的元素的质量比为1:1 | |
| B. | NaBH4既是氧化剂又是还原剂 | |
| C. | NaBH4是还原剂,水是氧化剂 | |
| D. | B被氧化,H被还原 |