题目内容
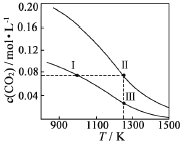
【题目】在体积均为1.0L的恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2mol CO2,在不同温度下反应CO2 (g)+C(s) ![]() 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中I、II、III点均处于曲线上)。下列说法正确的是
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中I、II、III点均处于曲线上)。下列说法正确的是
A. 反应CO2(g)+c(s)![]() 2CO(g) △H<0
2CO(g) △H<0
B. 体系的总压强P总:P总(状态Ⅱ)![]() 2P总(状态III)
2P总(状态III)
C. 体系中c(CO):6c(CO,状态I)<c(CO,状态II)
D. 从状态I到状态III的升温过程中,每一时刻,正逆反应速率:υ逆>υ正
【答案】B
【解析】分析:A项,升高温度c(CO2)减小,平衡向正反应方向移动,ΔH![]() 0;B项,状态II和状态III温度和体积相同,点II处于起始加入0.2molCO2的曲线上,点III处于起始加入0.1molCO2的曲线上,状态II起始加入的CO2物质的量是状态III的两倍,状态II相当于在状态III达平衡后将体积缩小一半,若平衡不移动,状态II总压强等于状态III的两倍,增大压强平衡逆向移动,P总(状态II)
0;B项,状态II和状态III温度和体积相同,点II处于起始加入0.2molCO2的曲线上,点III处于起始加入0.1molCO2的曲线上,状态II起始加入的CO2物质的量是状态III的两倍,状态II相当于在状态III达平衡后将体积缩小一半,若平衡不移动,状态II总压强等于状态III的两倍,增大压强平衡逆向移动,P总(状态II)![]() 2P总(状态III);C项,点I处于起始加入0.1molCO2的曲线上,点II处于起始加入0.2molCO2的曲线上,根据图像点I、点II平衡时c(CO2)平衡相等且
2P总(状态III);C项,点I处于起始加入0.1molCO2的曲线上,点II处于起始加入0.2molCO2的曲线上,根据图像点I、点II平衡时c(CO2)平衡相等且![]() 0.08mol/L,点I平衡时c(CO)=2[0.1-c(CO2)平衡],点II平衡时c(CO)=2[0.2-c(CO2)平衡], 则6c(CO,状态I)
0.08mol/L,点I平衡时c(CO)=2[0.1-c(CO2)平衡],点II平衡时c(CO)=2[0.2-c(CO2)平衡], 则6c(CO,状态I)![]() c(CO,状态II);D项,该反应为吸热反应,升温过程中υ正
c(CO,状态II);D项,该反应为吸热反应,升温过程中υ正![]() υ逆。
υ逆。
详解:A项,根据图像,升高温度c(CO2)减小,平衡向正反应方向移动,正反应为吸热反应,ΔH![]() 0,A项错误;B项,状态II和状态III温度和体积相同,点II处于起始加入0.2molCO2的曲线上,点III处于起始加入0.1molCO2的曲线上,状态II起始加入的CO2物质的量是状态III的两倍,状态II相当于在状态III达平衡后将体积缩小一半,若平衡不移动,状态II总压强等于状态III的两倍,增大压强平衡逆向移动,P总(状态II)
0,A项错误;B项,状态II和状态III温度和体积相同,点II处于起始加入0.2molCO2的曲线上,点III处于起始加入0.1molCO2的曲线上,状态II起始加入的CO2物质的量是状态III的两倍,状态II相当于在状态III达平衡后将体积缩小一半,若平衡不移动,状态II总压强等于状态III的两倍,增大压强平衡逆向移动,P总(状态II)![]() 2P总(状态III),B项正确;C项,点I处于起始加入0.1molCO2的曲线上,点II处于起始加入0.2molCO2的曲线上,根据图像点I、点II平衡时c(CO2)平衡相等且
2P总(状态III),B项正确;C项,点I处于起始加入0.1molCO2的曲线上,点II处于起始加入0.2molCO2的曲线上,根据图像点I、点II平衡时c(CO2)平衡相等且![]() 0.08mol/L,点I平衡时c(CO)=2[0.1-c(CO2)平衡],点II平衡时c(CO)=2[0.2-c(CO2)平衡],若c(CO2)平衡=0.08mol/L,则6c(CO,状态I)=c(CO,状态II),而c(CO2)平衡
0.08mol/L,点I平衡时c(CO)=2[0.1-c(CO2)平衡],点II平衡时c(CO)=2[0.2-c(CO2)平衡],若c(CO2)平衡=0.08mol/L,则6c(CO,状态I)=c(CO,状态II),而c(CO2)平衡![]() 0.08mol/L,则6c(CO,状态I)
0.08mol/L,则6c(CO,状态I)![]() c(CO,状态II),C项错误;D项,该反应为吸热反应,从状态I到状态III升温过程中υ正
c(CO,状态II),C项错误;D项,该反应为吸热反应,从状态I到状态III升温过程中υ正![]() υ逆,D项错误;答案选B。
υ逆,D项错误;答案选B。

【题目】某硫酸工业废渣的主要成分为SiO2、MgO、Al2O3、Fe2O3等。回收废渣中金属元素的工艺流程如下:
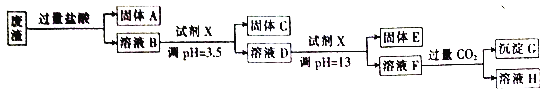
已知常温条件下:
①阳离子以氢氧化物形式开始沉淀和恰好完全沉淀(阳离子浓度等于10-5mol/L)时的pH如下表所示。
阳离子 | Fe3+ | A13+ | Mg2+ |
开始沉淀时的pH | 1.9 | 3.7 | 9.6 |
恰好完全沉淀时的pH | 3.2 | 5.2 | 11.0 |
②饱和氨水溶液中c(OH-)约为1×10-3mol/L。
请回答下列问题:
(1)固体C为________(填化学式)。
(2)上述流程中两次使用试剂X,试剂X是________(填“氨水”或“氢氧化钠”),其理由是________ 。
(3)向溶液D中滴人试剂X的过程中,发生反应的离子方程式有Mg2++2OH-=Mg(OH)2、________、________。
(4)溶液D→固体E的过程中需要控制溶液pH=13,如果pH过小,可能导致的后果是________。
(5)写出溶液F→溶液H的离子方程式: ________ 。
(6)Ksp[Mg(OH)2]= ________。