题目内容
【题目】密闭容器中充有10molCO与20molH2,在催化剂作用下反应生成甲醇:CO(g)+2H2(g)CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如图所示。下列说法正确的是( )
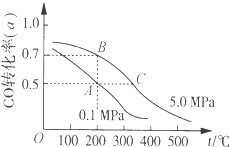
A.若A、B两点表示在某时刻达到的平衡状态,则A、B两点时容器内总气体的物质的量,n(A):n(B)=4:5
B.若A、C两点都表示已达到的平衡状态,则从反应开始至到达平衡状态所需的时间tA>tC
C.设B、C两点的平衡常数分别为KB、KC,则KB<KC
D.在不改变反应物用量的情况下,采取降温、减压或将甲醇从混合体系中分离出来均可提高CO的转化率
【答案】B
【解析】
A.A点CO的转化率为0.5,则参加反应的CO为10mol×0.5=5mol,则:
CO(g)+2H2(g)CH3OH(g)气体物质的量减少
1 2
5mol 10mol
故A点平衡时,混合气体总的物质的量=10mol+20mol-10mol=20mol;
B点CO的转化率为0.7,则参加反应的CO为10mol×0.7=7mol,则:
CO(g)+2H2(g)CH3OH(g)气体物质的量减少
1 2
7mol 14mol
故B点平衡时,混合气体总的物质的量=10mol+20mol-14mol=16mol;
故A、B两点时容器内总气体的物质的量之比n(A):n(B)=20mol:16mol=5:4,故A错误;
B.C点的温度、压强都高于A点,温度越高、压强越大,反应速率越快,最先到达平衡,故从反应开始至到达平衡状态所需的时间tA>tC,故B正确;
C.由图可知,一定压强下,温度越高,CO的转化率越低,说明升高温度平衡向逆反应方向移动,B的温度低于C点,故平衡常数KB>KC,故C错误;
D.正反应是气体体积减小的反应,减压平衡向逆反应方向移动,CO的转化率降低,故D错误;
答案为B。

 特高级教师点拨系列答案
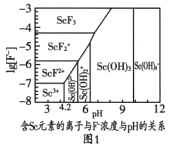
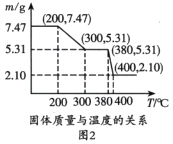
特高级教师点拨系列答案【题目】氧化锌工业品广泛应用于橡胶、涂料、陶瓷、化工、医药、玻璃和电子等行业,随着工业的飞速发展,我国对氧化锌的需求量日益增加,成为国民经济建设中不可缺少的重要基础化工原料和新型材料。用工业含锌废渣(主要成分为ZnO,还含有铁、铝、铜的氧化物,Mn2+、Pb2+、Cd2+等)制取氧化锌的工艺流程如图所示:

已知:相关金属离子c(Mn+)=0.1mol/L生成氢氧化物沉淀的pH如下表所示:
Fe3+ | Fe2+ | Al3+ | Mn2+ | Zn2+ | Cu2+ | Cd2+ | |
开始沉淀 | 1.5 | 6.3 | 3.4 | 8.1 | 6.2 | 6.0 | 7.4 |
沉淀完全 | 2.8 | 8.3 | 4.7 | 10.1 | 8.2 | 8.0 | 9.4 |
回答下列问题:
(1)为保证锌渣酸浸的充分,先保持酸过量,且c(H+)=0.5mol/L左右。写出一种加快锌渣浸出的方法:_______________
(2)为调节溶液的pH,则试剂X为__________________(填化学式),且调节溶液pH的范围是____________
(3)除杂时加入高锰酸钾的作用是_______________,发生反应的离子方程式为_____________
(4)“过滤”所得滤渣的主要成分是_____________________(填化学式)
(5)写出“碳化合成”的化学方程式:_____________________;“碳化合成”过程需纯碱稍过量,请设计实验方案证明纯碱过量:_____________________
【题目】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结 论 |
A | 将 | 生成了 |
B | 向浓度均为 |
|
C | 淀粉 | 还原性: |
D | 用pH试纸测得: |
|
A.AB.BC.CD.D