题目内容
【题目】铁被誉为“第一金属”,铁及其化合物广泛应用于生活、生产、国防等领域。
(1)Fe2+是构成人体血红蛋白(如图1所示)的重要元素,基态Fe2+简化的电子排布式为___________;用物质结构与性质知识分析Fe2+在空气中容易被氧化成Fe3+的主要原因:_________________________________________。
(2)血红蛋白中所含非金属元素的电负性由小到大的顺序为___________;碳原子的杂化轨道类型为__________________杂化。
(3)羰基铁[Fe(CO)5]可用作催化剂等。1mol[Fe(CO)5]分子中含有____mol的σ键,与CO互为等电子体的离子的化学式为___________________________(写一种)。
(4)据报道,工业上可电解熔融的FeO、Fe2O3冶炼高纯铁。Fe2O3的熔点____________(填“高于”或“低于”) FeO的熔点,理由是____________________________________________。
(5)铁晶体有面心立方、体心立方。在这两种晶体中铁的配位数之比为______________。
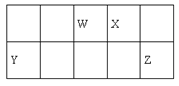
(6)某种氮化铁晶体的晶胞如图2所示。已知:该晶胞边长、高分别为anm、bnm,NA=6.02×1023mol-l
①该氮化铁晶体的化学式为______________。
②列式表示该氮化铁晶体的密度_________________________________________。

【答案】 [Ar]3d6 Fe3+的3d轨道半充满,较稳定,Fe2+容易被氧化为Fe3+ H、C、N、O sp3 、sp2 10 CN- 高于 Fe3+所带电荷数大于Fe2+,Fe3+的半径小于Fe2+,所以Fe2O3 的晶格能大于FeO,熔点高于FeO。 3:2 Fe3N 364/(3![]() NA a2b)g/nm3
NA a2b)g/nm3
【解析】本题主要考查物质结构。
(1)基态Fe2+简化的电子排布式为[Ar]3d6;用物质结构与性质知识分析Fe2+在空气中容易被氧化成Fe3+的主要原因:Fe3+的3d轨道半充满,较稳定,Fe2+容易被氧化为Fe3+。
(2)血红蛋白中所含非金属元素为H、C、N、O,同周期元素非金属性C<N<O,H的非金属性较弱,总之,非金属性H<C<N<O,所以电负性由小到大的顺序为H、C、N、O;单键碳原子的杂化轨道类型为sp3杂化,双键碳原子的杂化轨道类型为sp2杂化。
(3)[Fe(CO)5]分子中CO分子含有一个σ键,每个CO分子与Fe原子之间有一个σ键,共10个σ键,所以1mol[Fe(CO)5]分子中含有10mol的σ键,与CO互为等电子体的离子的化学式为CN-。
(4)Fe2O3的熔点高于FeO的熔点,理由是Fe3+所带电荷数大于Fe2+,Fe3+的半径小于Fe2+,所以Fe2O3的晶格能大于FeO,熔点高于FeO。
(5)铁的面心立方晶体中配位数是12,体心立方晶体中配位数是8。在这两种晶体中铁的配位数之比为3:2。
(6)①晶胞平均含有6个铁原子、2个氮原子,所以该氮化铁晶体的化学式为Fe3N。
②晶胞底面积为底面积为3![]() a2,晶胞体积为3
a2,晶胞体积为3![]() a2b,该氮化铁晶体的密度为364/(3
a2b,该氮化铁晶体的密度为364/(3![]() NA a2b)g/nm3。
NA a2b)g/nm3。

【题目】变量控制是科学研究的重要方法。相同质量的碳酸钙与足量1 mol·L-1盐酸分别在下列条件下发生反应,化学反应速率最大的是
选项 | 碳酸钙的状态 | 实验温度/℃ |
A | 粉末 | 10 |
B | 粉末 | 30 |
C | 块状 | 10 |
D | 块状 | 30 |
A.AB.BC.CD.D