题目内容
【题目】下列化学反应的离子方程式错误的是
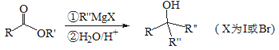
A.![]() 与盐酸反应:
与盐酸反应:![]()
B.![]() 溶于过量NaOH溶液: Al2O3+2OH-=2AlO2-+H2O
溶于过量NaOH溶液: Al2O3+2OH-=2AlO2-+H2O
C.铝溶于氢氧化钠溶液: 2Al+2OH-+2H2O=2AlO2-+3H2↑
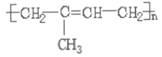
D.![]() 溶于NaOH溶液:
溶于NaOH溶液:![]()
【答案】D
【解析】
A.![]() 与盐酸反应生成氯化铝和水,反应的离子方程式为
与盐酸反应生成氯化铝和水,反应的离子方程式为![]() ,选项A正确;
,选项A正确;
B.![]() 溶于过量NaOH溶液生成偏铝酸钠和水,反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O,选项B正确;
溶于过量NaOH溶液生成偏铝酸钠和水,反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O,选项B正确;
C.铝溶于氢氧化钠溶液生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,选项C正确;
D.![]() 溶于NaOH溶液生成偏铝酸钠和水,反应的离子方程式为
溶于NaOH溶液生成偏铝酸钠和水,反应的离子方程式为![]() ,选项D错误;
,选项D错误;
答案选D。

 智能训练练测考系列答案
智能训练练测考系列答案【题目】某温度下,在 2 L 恒容密闭容器中 3 种物质间进行反应,X、Y、Z 的物质的量随时间的变化曲线如图所示,反应在 t1 min 时达到平衡。
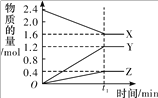
(1)请写出该反应的化学方程式:_____。
(2)若上述反应中X、Y、Z 分别为 NH3、H2、N2,在此 t1 min 时间内,用H2 表示该反应的平均速率 v(H2)为_____。
(3)拆开 1mol 共价键所需吸收的能量如下表:
共价键 | H-H | N≡N | N-H |
吸收的能量/kJ | 436 | 946 | 391 |
1mol N2 完全反应为NH3_____(填:吸收或放出)_____kJ 能量。事实上,将 1molN2 和3molH2 放在反应容器中,使它们充分反应,反应的热量变化总小于计算值,原因是_________。
(4)下列叙述能判断该反应达到平衡状态的是_____(填字母代号)。
A 容器内各气体组分的质量分数不再发生改变
B 正反应速率与逆反应速率相等
C 容器内气体的密度不再发生改变
D 混合气体的平均相对分子质量不再发生改变
【题目】一定温度下,10mL 0.40 mol·L-1H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 3 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是( )(溶液体积变化忽略不计)
A. 反应至6min时,H2O2分解了50%
B. 反应至6min时,c(H2O2)=0.20 mol·L-1
C. 0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L·min)
D. 4~6min的平均反应速率:v(H2O2)>3.3×10-2mol/(L·min)
【题目】X、Y、Z、W、R、P、Q是短周期主族元素,部分信息如表所示:
X | Y | Z | W | R | P | Q | |
原子半径/nm | 0.154 | 0.074 | 0.099 | 0.075 | 0.143 | ||
主要化合价 | -4,+4 | -2 | -1、+7 | -3、+5 | +3 | ||
其他 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
请完成下列问题:
(1)W在周期表中的位置是___,X与P形成的化合物的电子式___。
(2)R在自然界中有质量数为35和37的两种核素,它们之间的关系是互为___。
(3)Z与Q两元素的最高价氧化物水化物之间发生反应的离子方程式为___。
(4)Y与R相比,非金属性较强的是___(用元素符号表示),根据下列方法能证明这一结论的是___(填字母序号)。
A.常温下Y的单质呈固态,R的单质呈气态
B.R、Y的氢化物稳定性不同
.Y与R形成的化合物中的化合价
D.R、Y的氧化物的水化物的酸性强弱
(5)用电子式表示由Z和R组成的化合物的形成过程___。
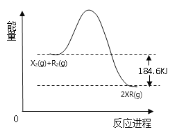
(6)如图为X2和R2燃烧反应的能量变化示意图,请根据此图写出该反应的热化学方程式为___(用物质化学式表示)。