题目内容
【题目】保存少量金属钠的方法是( )
A. 放在冰水中
B. 放在细沙中
C. 放在空气中
D. 放在煤油中
【答案】D
【解析】
根据金属钠的性质来分析其保存方法,钠性质较活泼,能和氧气、水等物质反应。
A、钠能和水反应生成氢氧化钠和氢气,所以钠不能保存在冰水中,选项A错误;B、细沙中有氧气,钠能和氧气发生生成氧化钠而变质,所以钠不能保存在细沙中,选项B错误;C、钠能和氧气发生生成氧化钠而变质,所以钠不能保存在空气中,选项C错误;D、钠的密度大于煤油的密度,且钠和煤油不反应,所以把钠放置在煤油中而阻止了与氧气和水的反应,选项D正确。答案选D。

 名校课堂系列答案
名校课堂系列答案【题目】在2 L密闭容器中,800 ℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=___________,已知:K(300 ℃)>K(350 ℃),该反应的逆反应是_______反应(填“放热”或“吸热”)。
(2)图中表示NO2的变化的曲线是____________,用O2的浓度变化表示从0~2 s内该反应的平均速率v=_____________。
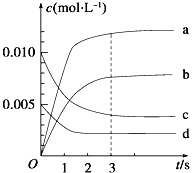
(3)能说明该反应已经达到平衡状态的是________。
a v(NO2)=2v(O2) b 容器内压强保持不变
c v逆(NO)=2v正(O2) d 容器内物质的密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a 及时分离出NO2气体 b 适当升高温度
c 选择高效的催化剂 d 增大O2的浓度
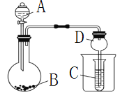
【题目】表中a、b、c表示相应仪器中加入的试剂,可用如图所示装置制取、净化、收集的气体是 ( )
编号 | 气体 | a | b | c |
A | NH3 | 浓氨水 | 生石灰 | 碱石灰 |
B | SO2 | 70%浓H2SO4 | Na2SO3固体 | 98%浓H2SO4 |
C | NO | 稀HNO3 | 铜屑 | H2O |
D | NO2 | 浓HNO3 | 铜屑 | NaOH溶液 |
A. A B. B C. C D. D