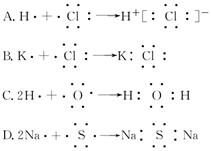题目内容
以下说法正确的是
| A.C60与金刚石一样属于原子晶体 |
| B.干冰升华破坏了共价键 |
| C.共价化合物中一定不含离子键 |
| D.氯化氢溶于水能电离出H+、Cl—,所以氯化氢是离子化合物 |
C
C60是分子晶体,干冰形成的晶体也是分子晶体,升华是物理变化,破坏的是分子间作用力。全部由共价键形成的化合物是共价化合物,所以共价化合物中不能出现离子键。在水溶液中能电离出离子的化合物不一定是离子化合物,只有在熔融状态下能导电的化合物才是离子化合物,氯化氢在熔融状态下不能导电,是共价化合物。答案选C。

练习册系列答案
相关题目