题目内容
下面是用电子式表示某些物质的形成过程,其中正确的是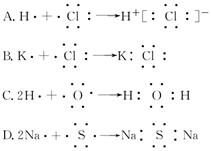
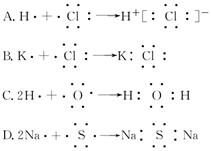
氯化氢是共价化合物,正确的是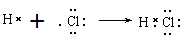 。氯化钾和硫化钠都是离子化合物,正确的分别为
。氯化钾和硫化钠都是离子化合物,正确的分别为 。
。 。水水极性键形成的共价化合物,C正确。答案选C。
。水水极性键形成的共价化合物,C正确。答案选C。
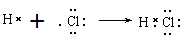 。氯化钾和硫化钠都是离子化合物,正确的分别为
。氯化钾和硫化钠都是离子化合物,正确的分别为 。
。 。水水极性键形成的共价化合物,C正确。答案选C。
。水水极性键形成的共价化合物,C正确。答案选C。
练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
题目内容
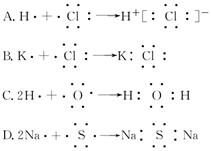
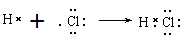 。氯化钾和硫化钠都是离子化合物,正确的分别为
。氯化钾和硫化钠都是离子化合物,正确的分别为 。
。 。水水极性键形成的共价化合物,C正确。答案选C。
。水水极性键形成的共价化合物,C正确。答案选C。
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案