题目内容
【题目】下列有关化学用语的表示中,正确的是
①氚的原子符号为![]()
②S2-的结构示意图为
③Na2O2的电子式为![]()
④用电子式表示CaCl2的形成过程为![]()
⑤NH3的结构式为![]()
⑥丙烷分子的球棍模型示意图为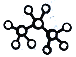
A. ①③⑤⑥ B. ①③④⑤ C. ①②⑤⑥ D. ②④⑤⑥
【答案】A
【解析】①氚的质子数是1,质子数是2;
②硫离子的核外电子数是18;
③过氧化钠是离子化合物,含有离子键;
④氯化钙是离子化合物;
⑤氨气分子中含有3个N-H键;
⑥球棍模型用来表现化学分子的三维空间分布。棍代表共价键,球表示构成有机物分子的原子。
①氚的质量数是3,原子符号为![]() ,正确;
,正确;
②S2-的结构示意图为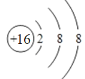 ,错误;
,错误;
③Na2O2是含有离子键的离子化合物,电子式为![]() ,正确;
,正确;
④用电子式表示CaCl2的形成过程为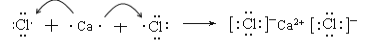 ,错误;
,错误;
⑤NH3的结构式为![]() ,正确;
,正确;
⑥丙烷分子的结构简式为CH3CH2CH3,球棍模型示意图为 ,正确。
,正确。
答案选A。

 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案【题目】下表是25 ℃时某些弱酸的电离平衡常数。
化学式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 | Ka1=5.9×10-2 |
(1)H2C2O4与含等物质的量的KOH的溶液反应后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为。
(2)向0.1 mol·L-1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=。
(3)向碳酸钠溶液中滴加少量氯水的离子方程式为。
(4)若0.1mol·L-1CH3COOH溶液与0.1mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则c(Na+)-c(CH3COO-)=mol·L-1(填精确计算结果)。
(5)将CH3COOH溶液与大理石反应所产生的标况下44.8L气体全部通入到2L 1.5mol/L的NaOH溶液中充分反应,则溶液中所有离子的物质的量浓度由大到小的顺序为。
