��Ŀ����
����Ŀ����10.0mL0.10mol��L-1��ˮ�е���10 mL0��1 mol��L��1���ᣬ��Һ��PH����������������ϵ��ͼ��ʾ�������������Ƴ����������й�������ȷ����
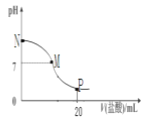
A��M-N��һ������c��Cl-��>c��NH4+��>c��OH-��>c��H+��
B��M���Ӧ���������Ϊ10.0mL
C��PH=7��Һ�д���c��Cl-��=c��NH4+��=c��OH-��=c��H+��
D��p�㴦����Һ�д��ڣ�2c��NH4+��+2c��NH3H2O��=c��Cl-��
���𰸡�D
��������
�����������10.0mL 0.10mol��L-1��ˮ�е���0.10mol��L1�����ᣬ��Һ��pH����������������ϵ��ͼ��ʾ��A��M-N�䰱ˮ��������Һ�ǰ�ˮ���Ȼ�淋Ļ����Һ��һ������c��NH4+����c��Cl������c��OH������c��H+����A����B�����M���Ӧ������������10mL����ô�õ������Ȼ����Һ����ʱ��Һ��pH<7����M���pH=7��Ӧ���ǰ�ˮ������B����C��pH��7��Һ����c��H+��=c��OH���������ݵ���غ���c��NH+ 4��=c��Cl����������c��NH4+��= c��Cl������c��H+��=c��OH������C����D��P����������غ���2c��NH4+��+2c��NH3H2O��=c��Cl������D��ȷ����ѡD��

 �����ߴ���ϵ�д�
�����ߴ���ϵ�д�