题目内容
【题目】已知Ksp(AgCl) = 1.56 × 10-10, Ksp(AgBr) = 7.7 × 10-13,Ksp(Ag2CrO4) = 9.0× 10-12.某溶液中含有Cl-、Br-和CrO42-浓度均为0.010molL-1,向该溶液中逐滴加入0.010molL-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
A.Cl-、Br-、CrO42-
B.CrO42-、Br-、Cl-
C.Br-、Cl-、CrO42-
D.Br-、CrO42-、Cl-
【答案】C
【解析】
试题分析:在一定温度下,在难溶化合物的饱和溶液中组成沉淀的各离子的浓度的乘积是一常数,称溶度积常数。根据AgCl、AgBr和Ag2CrO4的Ksp可知开始沉淀时需要银离子的浓度分别为
c(Ag+)=![]() =
=![]() =1.56×10-8
=1.56×10-8
c(Ag+)=![]() =
=![]() =7.7×10-11
=7.7×10-11
c(Ag+)=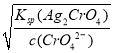 =
=![]() =3.0×10-5
=3.0×10-5
根据计算可知,三种离子产生沉淀的先后顺序为Br-、Cl-、CrO42-,答案选C。

练习册系列答案
相关题目