��Ŀ����
����Ŀ���̲IJ�ͼ���м������ں��ḻ���ص㡣��ش��������⣺
��1���������ڵ�ij����Ԫ�أ����һ�����������������ͼ1��ʾ�����Ԫ�ض�Ӧ��ԭ����___�ֲ�ͬ�˶�״̬�ĵ��ӡ�



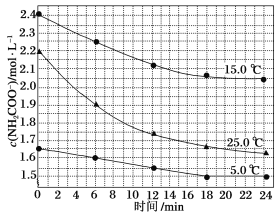
��2����ͼ2��ʾ��ÿ�����߱�ʾ���ڱ���A-��A�е�ijһ��Ԫ���⻯��ķе�仯��ÿ��С�ڵ����һ���⻯�����a���������___��
��3��CO2�ڸ��¸�ѹ�����γɵľ����侧����ͼ3��ʾ����þ������������___���塣
��4����һ�����ܽ���Al��P֮��ĵ�������Ԫ����___�֡�GaCl3ԭ�ӵ��ӻ���ʽΪ___��
��5�������ɱ����ⶼ�Ƿ��Ӿ��壬���Ľṹ���������ԣ����ɱ�����ľ���������ƵĽṹ�������ɱ�������һ��������Χ��___�����ڷ��ӡ�D�Ĵ����ξ���ֲ��ṹ��ͼ���þ����к��еĻ�ѧ����___������ĸ��ţ���

a�����Լ� b���Ǽ��Լ� c����λ�� d��������
���𰸡�12 SiH4 ԭ�� 3 sp2�ӻ� 12 abc
��������
��1���������ͼ���������Ԫ�ص���������ԶԶ���ڵڶ������ܣ�˵����Ԫ�ص�ԭ�Ӽ۵�����Ϊ2��ΪþԪ�أ�������12�ֲ�ͬ�˶�״̬�ĵ��ӡ�
��2���ڢ�A����A�е��⻯���NH3��H2O��HF����Ӽ����������ʷе����ͬ��������Ԫ���⻯��ķе㣬ֻ�Т�A��Ԫ���⻯�ﲻ���ڷ������������ṹ���ƣ���Է�����Խ���Ӽ�������Խ�е�Խ�ߣ�a���������߶�Ӧ������̬�⻯��SiH4��
��3����CO2�ڸ��¸�ѹ�����γɵľ���ͼ���Կ������侧��ṹΪ�ռ�����ṹ��ÿ��Cԭ����Χͨ�����ۼ�����4��Oԭ�ӣ����Ըþ���Ϊԭ�Ӿ��塣
��4����һ�����ܽ���Al��P֮��ĵ�������Ԫ����þ���衢��3�֣�GaCl3������ԭ�ӵļ۲���Ӷ�����3���Ҳ����ڹ¶Ե��ӣ�ԭ�ӵ��ӻ���ʽΪsp2�ӻ���
��5�����ݸɱ��ľ����ṹ��֪���ڸɱ�������ÿ��CO2������Χ���ڵ� CO2������12������D�Ĵ����ξ���ֲ��ṹ֪���þ����к��еĻ�ѧ���м��Լ����Ǽ��Լ�����λ����ѡabc��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��E��F�����ܱ������У���һ�������·�����Ӧ��E(s)+4F(g)![]() G(g)����֪�÷�Ӧ��ƽ�ⳣ��ֵ���±���ʾ������˵����ȷ����
G(g)����֪�÷�Ӧ��ƽ�ⳣ��ֵ���±���ʾ������˵����ȷ����
�¶ȡ� | 25 | 80 | 230 |
ƽ�ⳣ��ֵ | 5��104 | 2 | 1.9�� 10��5 |
A.������Ӧ��������Ӧ
B.25��ʱ����ӦG(g)![]() E(s)+4F(g)��ƽ�ⳣ��ֵ��0.5
E(s)+4F(g)��ƽ�ⳣ��ֵ��0.5
C.��80��ʱ�����ijʱ�̣�F��GŨ�Ⱦ�Ϊ0.5 mol��L��1�����ʱv(��)��v(��)
D.���º����£����������ٳ�������G(g)������ƽ��ʱ��G������ٷֺ���������