题目内容
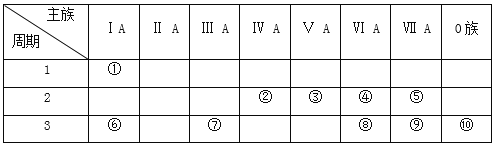
【题目】同周期的两种主族元素A和B能够形成离子化合物AmBn , 已知A的原子序数为a,则B的原子序数可能为( )
A.a+8+m﹣n
B.a+16﹣m+n
C.a+24﹣m﹣n
D.a+18﹣m﹣n
【答案】D
【解析】解:同周期的两种主族元素A和B能够形成离子化合物AmBn , 则A为金属元素,B为非金属元素,已知A的原子序数为a,则离子中A少了一个电子层,B的电子层不变,
若在短周期,A的原子序数为a,则B的原子序数为(a﹣m)+8﹣n=a+8﹣m﹣n,
若在四、五周期,A的原子序数为a,则B的原子序数为(a﹣m)+18﹣n=a+18﹣m﹣n,
故选D.

 考前必练系列答案
考前必练系列答案【题目】人们常常利用化学反应中的能量变化为人类服务。
(1)氢能是一种具有发展前景的理想清洁能源,氢气燃烧时放出大最的热。氢气燃烧生成水蒸气的能最变化如下图所示:
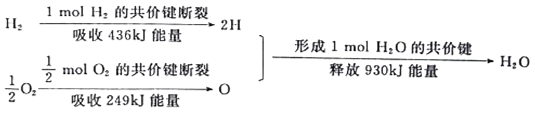
根据上图可知,在化学反应中,不仅存在物质的变化,而且伴随着______变化,1molH2完全燃烧生成1molH2O(气态)时,释放的能量是_______kJ。
(2)下列化学反应在理论上可以设计成原电池的是________。
A.Fe+2FeCl3=3FeCl2 B.SO3+H2O=H2SO4
C.CH4+2O2![]() CO2+2H2O D.Ba(OH)2+H2SO4=BaSO4+2H2O
CO2+2H2O D.Ba(OH)2+H2SO4=BaSO4+2H2O
(3)下图是某兴趣小组设计的原电池示意图,实验结束后,在实验报告上记录信息如下:
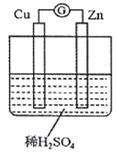
a.电流计指针偏转 |
b.Cu极有H2产生 |
c.H+向负极移动 |
d.电流由Zn经导线流向Cu |
①实验报告中记录合理的是_______(填序号)。
②请写出该电池的负极反应式_________。
③若有1mol电子流过导线,则理论上产生H2的质量为______g.
④将稀H2SO4换成CuSO4溶液,电极质量增加的是______(填“锌极”或“铜极”,下同),溶液中SO42-移向_______。