��Ŀ����
����Ŀ��������Ҫ�ĵ��ʣ��ϳ�ԭ��Ϊ��N2��g��+3H2��g�� ![]() 2NH3��g����H=��92.4kJ/mol���ش��������⣺
2NH3��g����H=��92.4kJ/mol���ش��������⣺
��1��д��ƽ�ⳣ��K�ı���ʽ �� ��������¶ȣ��÷�ӦKֵE����ѧ��Ӧ���� �� N2��ת���������������С�����䡱����
��2����500�桢20MPaʱ����N2��H2����һ���ݻ�Ϊ2L���ܱ������з�����Ӧ����Ӧ�����и������ʵ����仯��ͼ��ʾ���ش��������⣺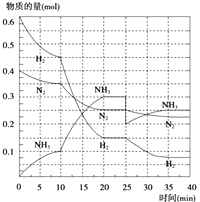
��10min����NH3��ʾ��ƽ����Ӧ���ʣ� ��
����10��20min�ڣ�NH3Ũ�ȱ仯��ԭ�������
A�����˴��� B����С�������
C�������¶� D������NH3���ʵ���
�۵�1��ƽ���ʱ��Ϊ�� �� ��2��ƽ���ʱ��Ϊ�� �� ��1��ƽ�⣺ƽ�ⳣ��K1= �������ݵı���ʽ������2��ƽ��ʱNH3�����������
���ڷ�Ӧ������25minʱ�����߷����仯��ԭ�� ��
��ڶ���ƽ��ʱ����ƽ���ƽ�ⳣ��K2K1 �� ������ڡ�����С�ڡ����ڡ�����
���𰸡�
��1��K= ![]() ,��С,����
,��С,����
��2��0.005mol/��L��min��,A,20��25min,35��40min,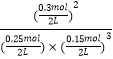 ,45.5%,����0.1molNH3,����
,45.5%,����0.1molNH3,����
���������⣺��1����ѧƽ�ⳣ����ƽ��ʱ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ������N2��g��+3H2��g�� ![]() 2NH3��g�����÷�Ӧ��ƽ�ⳣ������ʽK=
2NH3��g�����÷�Ӧ��ƽ�ⳣ������ʽK= ![]() ����ѧ��Ӧ���¶ȵ����߷�Ӧ���ʼӿ죬���¶ȵĽ��ͣ���Ӧ���ʼ��������Խ����¶Ȼ�Ѩ��Ӧ���ʼ�������ѧƽ��ķ�Ӧ�������¶������ȵķ����ƶ����÷�Ӧ����ӦΪ���ȷ�Ӧ�������¶ȣ���ѧƽ��������Ӧ�����ƶ������Ե�����ת��������
����ѧ��Ӧ���¶ȵ����߷�Ӧ���ʼӿ죬���¶ȵĽ��ͣ���Ӧ���ʼ��������Խ����¶Ȼ�Ѩ��Ӧ���ʼ�������ѧƽ��ķ�Ӧ�������¶������ȵķ����ƶ����÷�Ӧ����ӦΪ���ȷ�Ӧ�������¶ȣ���ѧƽ��������Ӧ�����ƶ������Ե�����ת��������
���Դ��ǣ� ![]() �����٣�����
�����٣�����
��2���ٸ��ݷ�Ӧ����v��NH3��= ![]() =
= ![]() =0.005mol/��L��min��������ͼ���֪��������ʵ����仯���ӣ���10minʱ�仯�������ģ�20min��ƽ��ʱ����n��N2��=0.025mol��4=0.1mol����n��H2��=0.025mol��12=0.3mol����n��NH3��=0.025mol��8=0.2mol�����ʵ����仯֮�ȵ��ڻ�ѧ������֮�ȣ������������ʵ��������ӱ�����ͬ��˵��10min���ܸı��������ʹ�ô�������С����൱������ѹǿ��Ӧ�÷�Ӧ����������ӱ��������¶ȣ�Ӧ�÷�Ӧ���ʼ�С������NH3���ʵ������淴Ӧ�������ӵı�����ֻ��ʹ�ô������ϣ�����ͼ����Կ���������Ӧ���е�ʱ20��25min�������ʵ������䣬˵����Ӧ�ﵽƽ��״̬����ѧƽ�ⳣ������������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ���ͼ���֪��20min��ƽ��ʱ��n��N2��=0.025mol��10=0.25mol��n��H2��=0.025mol��6=0.15mol��n��NH3��=0.025mol��12=0.3mol������������ƽ�ⳣ��K= C 2 ( N H 3 ) C ( N 2 ) C 3 ( H 2 ) = ( 0.3 m o l 2 L ) 2 ( 0.25 m o l 2 L ) �� ( 0.15 m o l 2 L ) 3 =426.7����2��ƽ��ʱNH3���������= 2.5 m o l 2.5 m o l + 2.25 m o l + 0.75 m o l ��100%=45.5%���ܵ�25���ӣ�NH3�����ʵ���ͻȻ���٣���H2��N2�����ʵ������䣬˵��Ӧ�Ƿ����NH3����ͼ����Կ���������Ӧ���е�ʱ35��40min�������ʵ������䣬˵����Ӧ�ﵽ�ڶ���ƽ��״̬��ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ��䣬ƽ�ⳣ�����䣬���Գ�ȥ0.1mol������ʱƽ�ⳣ��K�����䣻
=0.005mol/��L��min��������ͼ���֪��������ʵ����仯���ӣ���10minʱ�仯�������ģ�20min��ƽ��ʱ����n��N2��=0.025mol��4=0.1mol����n��H2��=0.025mol��12=0.3mol����n��NH3��=0.025mol��8=0.2mol�����ʵ����仯֮�ȵ��ڻ�ѧ������֮�ȣ������������ʵ��������ӱ�����ͬ��˵��10min���ܸı��������ʹ�ô�������С����൱������ѹǿ��Ӧ�÷�Ӧ����������ӱ��������¶ȣ�Ӧ�÷�Ӧ���ʼ�С������NH3���ʵ������淴Ӧ�������ӵı�����ֻ��ʹ�ô������ϣ�����ͼ����Կ���������Ӧ���е�ʱ20��25min�������ʵ������䣬˵����Ӧ�ﵽƽ��״̬����ѧƽ�ⳣ������������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ���ͼ���֪��20min��ƽ��ʱ��n��N2��=0.025mol��10=0.25mol��n��H2��=0.025mol��6=0.15mol��n��NH3��=0.025mol��12=0.3mol������������ƽ�ⳣ��K= C 2 ( N H 3 ) C ( N 2 ) C 3 ( H 2 ) = ( 0.3 m o l 2 L ) 2 ( 0.25 m o l 2 L ) �� ( 0.15 m o l 2 L ) 3 =426.7����2��ƽ��ʱNH3���������= 2.5 m o l 2.5 m o l + 2.25 m o l + 0.75 m o l ��100%=45.5%���ܵ�25���ӣ�NH3�����ʵ���ͻȻ���٣���H2��N2�����ʵ������䣬˵��Ӧ�Ƿ����NH3����ͼ����Կ���������Ӧ���е�ʱ35��40min�������ʵ������䣬˵����Ӧ�ﵽ�ڶ���ƽ��״̬��ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ��䣬ƽ�ⳣ�����䣬���Գ�ȥ0.1mol������ʱƽ�ⳣ��K�����䣻
���Դ��ǣ�0.005mol/��L��min����A��20��25min��35��40min�� 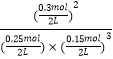 ��45.5%�������0.1molNH3�����ڡ�
��45.5%�������0.1molNH3�����ڡ�
�����㾫����������Ҫ�����˷�Ӧ���ʵĶ�����ʾ�����ͻ�ѧƽ�ⳣ���ĺ�������֪ʶ�㣬��Ҫ���շ�Ӧ���ʵĵ�λ��mol/(L��min)��mol/(L��s) v=��c-��t��ָ��һ�������µĿ��淴Ӧ�����Ӧ���淴Ӧ��������ȣ���Ӧ������и���ֵ�Ũ�Ȳ����״̬������ȷ�����⣮

 ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�����Ŀ���±���Ԫ�����ڱ���һ���֣�������ŷֱ����ijһԪ�ء���ش��������⣮
���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
2 | �� | �� | �� | �� | ||||
3 | �� | �� | �� | �� | �� | �� |
��1�������뵼����ϵ�Ԫ���� ______����Ԫ�ط��ţ���
��2����̬�⻯����������������ˮ�����ֱ�ӻ�������һ���ε�Ԫ���� ______�������ƣ���
��3���������������Ӱ뾶��С����___________�������ӷ��ţ���
��4���� ~ �������������ˮ�����У�������ǿ���� __________���ѧʽ����������ǿ����________���ѧʽ�������������������ˮ���ﷴӦ�����ӷ���ʽΪ__________��
��5���ࡢ����γ�A2B2�͵Ĺ��ۻ���������ж��߾�����8�����ȶ��ṹ���������ʽΪ_________________��



