题目内容
【题目】稀释0.1mol·L-1的CH3COOH溶液过程中,以下各项数值增大的是()
A.n(H+)B.c(CH3COO-)
C.![]() D.
D.![]()
【答案】A
【解析】
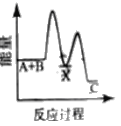
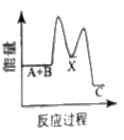
A项、稀释0.1mol·L-1的CH3COOH溶液过程中,电离平衡右移,溶液中n(H+)增大,故A正确;
B项、稀释0.1mol·L-1的CHCOOH溶液过程中,电离平衡右移,溶液中n(CH3COO-)增大,由于体积增大,c(CH3COO-)减小,故B错误;
C项、CH3COOH溶液中电离常数Ka=![]() ,
,![]() =
=![]() ,稀释过程中,温度不变,电离常数Ka不变,c(H+)减小,
,稀释过程中,温度不变,电离常数Ka不变,c(H+)减小,![]() 减小,则
减小,则![]() 减小,故C错误;
减小,故C错误;
D项、CH3COOH溶液中电离常数Ka=![]() ,稀释过程中,温度不变,电离常数Ka不变,故D错误;
,稀释过程中,温度不变,电离常数Ka不变,故D错误;
故选A。

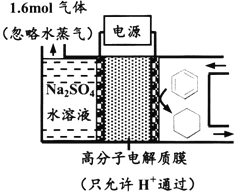
【题目】工业上用含三价钒(V2O3)为主的某石煤为原料(含有 Al2O3、CaO 等杂质),钙化法焙烧制备 V2O5,其流程如下:
![]()
(资料)+5 价钒在溶液中的主要存在形式与溶液 pH 的关系:
pH | 4~6 | 6~8 | 8~10 | 10~12 |
主要离子 | VO2+ | VO3- | V2O74- | VO43- |
(1)焙烧: 向石煤中加生石灰焙烧,将 V2O3 转化为 Ca(VO3)2 的化学方程式是______________。
(2)酸浸:①Ca(VO3)2 难溶于水,可溶于盐酸。若焙砂酸浸时溶液的 pH=4,Ca(VO3)2 溶于盐酸的离子方程式是________。
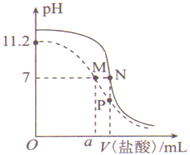
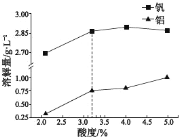
②酸度对钒和铝的溶解量的影响如图所示:酸浸时溶液的酸度控制在大约 3.2%,根据下图推测,酸浸时不选择更高酸度的原因是________________。
(3)转沉: 将浸出液中的钒转化为 NH4VO3 固体,其流程如下:
![]()
①浸出液中加入石灰乳的作用是_____。
②向(NH4)3VO4 溶液中加入 NH4Cl 溶液,控制溶液的 pH=7.5。当 pH>8 时,NH4VO3 的产量明显降低,原因是_______________。
(4)测定产品中 V2O5 的纯度:称取 ag 产品,先用硫酸溶解,得到(VO2)2SO4 溶液。再加入 b1mLc1mol/L(NH4)2Fe(SO4)2 溶液(VO2++2H++Fe2+=VO2++Fe3++H2O) 最后用 c2mol/LKMnO4 溶液滴定过量的(NH4)2Fe(SO4)2 至终点,消耗 KMnO4 溶液的体积为 b2mL。已知 MnO4-被还原为 Mn2+,假设杂质不参与反应。则产品中 V2O5 的质量分数是_____。(V2O5 的摩尔质量::182g/mol)