题目内容
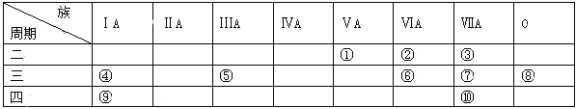
【题目】下表是元素周期表的一部分,针对表中的①~⑨ 种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是: (填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是 ,碱性最强的化合物的电子式是: 。
(3) 最高价氧化物是两性氧化物的元素是 ;写出它的氧化物与氢氧化钠反应的离子方程式 。
(4)用电子式表示元素④与⑥形成的的化合物的形成过程 ,该化合物属于 (填“共价”或“离子”)化合物。
(5)元素①的氢化物的电子式为 ,该化合物是由 (填“极性”或“非极性”)键形成的。
【答案】(1)Ar
(2)HClO4;![]()
(3)Al ;Al2O3+2OH-=2AlO2-+H2O
(4)![]() ;离子
;离子
(5)![]() ;极性
;极性
【解析】试题分析:根据元素在周期表中的位置可知①~⑨元素分别是N、O、F、Na、Al、S、Cl、Ar、K、Br。
(1)在这些元素中,化学性质最不活泼的是稀有气体元素Ar;
(2)非金属性越强,最高价含氧酸的酸性越强,F没有含氧酸,则在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4;K的金属性最强,则氢氧化钾的碱性最强,氢氧化钾是含有离子键和共价键的离子化合物,电子式是![]() ;
;
(3)最高价氧化物是两性氧化物的元素是Al,它的氧化物与氢氧化钠反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O;
(4)元素④与⑥形成的的化合物是硫化钠,含有离子键的离子化合物,其形成过程可表示为![]() ;
;
(5)元素①的氢化物是氨气,含有共价键的共价化合物,电子式为![]() ,N和H是不同的非金属,则该化合物是由极性键形成的。
,N和H是不同的非金属,则该化合物是由极性键形成的。

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目