题目内容
【题目】如图的实验装置可用于研究SO2转化为SO3的转化率。已知:SO3的熔点是16.8℃,沸点是44.8℃处为SO2气体发生装置,C处为SO2与O2反应的装置。
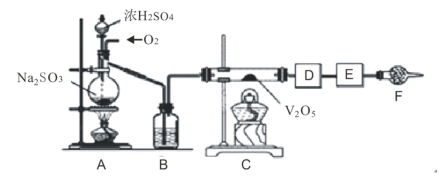
完成下列填空:
(1)A处的化学反应方程式为___,所用的硫酸一般为___(此处填98%的硫酸溶液、70%的硫酸溶液或30%的硫酸溶液)。
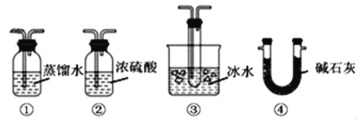
(2)根据实验需要,应该在D、E处连接合适的装置。请从图中选择,将所选装置的序号填入相应的空格,D:___,E:____。
(3)用12.6gNa2SO3粉末与足量浓硫酸进行此实验,当A处反应结束时,再继续通入一段时间![]() ,最后测得E处装置增重1.28gSO2,则此时SO2的转化率为____%。
,最后测得E处装置增重1.28gSO2,则此时SO2的转化率为____%。
(4)若Na2SO3变质,会影响到SO2的转化。现欲检验某Na2SO3样品是否变质,你的方法是___。
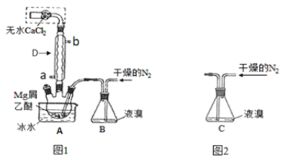
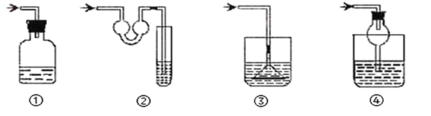
(5)以下各种尾气吸收装置中,适合于吸收该尾气,而且能防止倒吸的是___。
【答案】Na2SO3(s)+H2SO4(浓)=Na2SO4+SO2↑+H2O 70%硫酸溶液 ③ ④ 80% 取待测样品少许于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴加氯化钡溶液,如有白色沉淀生成,则证明样品变质,若无白色沉淀生成,证明样品未变质 ②④
【解析】
(1)A处浓硫酸与亚硫酸钠反应生成二氧化硫、硫酸钠和水;浓硫酸的浓度不需要太大,不形成酸雾、且吸收水即可;
(2)SO3的熔点是16.8℃,沸点是44.8℃,当温度低于 16.8℃时,三氧化硫以晶体状态存在,过量二氧化硫用碱吸收;
(3)最后测得E处装置增重,为剩余二氧化硫的质量;
(4)欲检验某Na2SO3样品是否变质,即检验硫酸根离子是否存在;
(5)具有球形结构、缓冲装置、固液不接触时可吸收尾气,且防止倒吸。
(1)A处的化学反应方程式为Na2SO3(s)+H2SO4(浓)=Na2SO4+SO2↑+H2O,浓硫酸的浓度不需要太大,可选70%的硫酸溶液,
故答案为:Na2SO3(s)+H2SO4(浓)=Na2SO4+SO2↑+H2O;70%的硫酸溶液;
(2)SO3的熔点是16.8℃,沸点是44.8℃,当温度低于 16.8℃时,三氧化硫以晶体状态存在,二氧化硫、三氧化硫的尾气处理用碱吸收,可知D中选③冷却,E中选④吸收未反应的二氧化硫,
故答案为:③;④;
(3)Na2SO3粉末的物质的量为![]() =0.1mol,与足量浓硫酸反应生成0.1molSO2,最后测得E处装置增重1.28g,为剩余二氧化硫的质量,其物质的量为
=0.1mol,与足量浓硫酸反应生成0.1molSO2,最后测得E处装置增重1.28g,为剩余二氧化硫的质量,其物质的量为![]() =0.02mol,则此时SO2的转化率为
=0.02mol,则此时SO2的转化率为![]() ×100%=80%,
×100%=80%,
故答案为:80%;
(4)若Na2SO3变质,会影响到SO2的转化。现欲检验某Na2SO3样品是否变质,检验方法为取待测样品少许于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴加氯化钡溶液,如有白色沉淀生成,则证明样品变质,若无白色沉淀生成,证明样品未变质,
故答案为:取待测样品少许于试管中,加适量蒸馏水配成溶液,先滴入足量稀盐酸,再滴加氯化钡溶液,如有白色沉淀生成,则证明样品变质,若无白色沉淀生成,证明样品未变质;
(5)装置②、④均属于防倒吸装置,所以适合于吸收该尾气,且能防止倒吸,①中装置密封易导致气体过多发生爆炸、③中倒扣的漏斗在液面下不能防止倒吸;
故答案为:②④。

【题目】根据下列实验及其现象,所得出的结论合理的是( )
选项 | 实验 | 现象 | 结论 |
A | 向 | 先有白色沉淀生成,后有蓝色絮状沉淀生成 | Ksp: |
B | 用pH试纸分别检验等浓度 | 前者试纸变蓝比后者更深些 |
|
C | 分别加热蒸干 | 前者能得到 |
|
D | 向某钠盐中滴加盐酸,产生的气体通入品红溶液 | 品红溶液褪色 | 该钠盐为 |
A.AB.BC.CD.D