题目内容
【题目】硫化钠在无机制备、废水处理等领域常用作沉淀剂,其水溶液称为“臭碱”。可在特殊条件下以硫酸钠固体与炭粉为原料制备:Na2SO4+2C ![]() Na2S+2CO2↑
Na2S+2CO2↑

(1)硫化钠固体在保存时需注意_________,原因是___________。
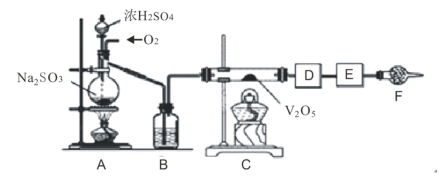
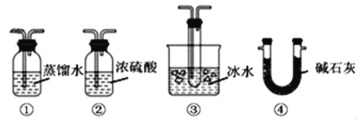
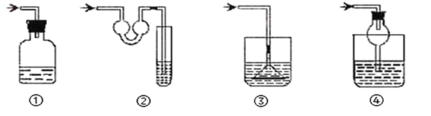
(2)实验室用上图装置以Na2SO4与炭粉为原料制备Na2S并检验气体产物、进行尾气处理。步骤如下:
①连接仪器顺序为__________(按气流方向,用小写字母表示);
②检查装置气密性;③装入固体药品及试剂,连好装置;
④加热,进行实验。
(3)若amolNa2SO4 和 2amolC按上述步骤充分反应,实际得到 Na2S小于 amol,则实验改进方案是____。某同学从氧化还原角度分析固体产物中可能含有少量 Na2SO3,请设计实验证明其猜测是否合理(供选择的试剂有:酚酞溶液、硝酸、稀盐酸、蒸馏水)_____。
(4)经实验测定,硫酸钠与炭粉在一定条件下反应还可生成等物质的量的两种盐和体积比为1︰3的 CO2 和CO两种气体。反应方程式为_______。
【答案】干燥环境密闭保存 硫化钠在空气中易被氧化,潮湿环境易水解 a→e→f→d 加入稍过量的碳 取少量反应后的固体于试管中,加蒸馏水溶解,滴加适量稀盐酸,若出现淡黄色沉淀,则固体中含亚硫酸钠,反之不含 2Na2SO4+4C![]() Na2S+Na2SO3+3CO↑+CO2↑
Na2S+Na2SO3+3CO↑+CO2↑
【解析】
(1)硫化钠易被氧化,溶液中硫离子可发生水解;
(2)A中发生Na2SO4+2C![]() Na2S+2CO2↑,选装置D检验二氧化碳,选装置C吸收尾气,二氧化碳不需要干燥;
Na2S+2CO2↑,选装置D检验二氧化碳,选装置C吸收尾气,二氧化碳不需要干燥;
(3)实际得到Na2S小于amol,可增大反应物的量;固体产物中可能含有少量Na2SO3,加盐酸发生氧化反应生成S;
(4)硫酸钠与炭粉在一定条件下反应还可生成等物质的量的两种盐和体积比为1:3的CO2和CO两种气体,C失去电子,S得到电子,结合电子、原子守恒来解答。
(1)硫化钠固体在保存时需注意干燥环境密闭保存,原因是硫化钠在空气中易被氧化,潮湿环境易水解;
(2)①A为制备装置,装置D检验二氧化碳,选装置C吸收尾气,则连接仪器顺序为a→e→f→d;
(3)若a mol Na2SO4和2a mol C按上述步骤充分反应,实际得到Na2S小于amol,则实验改进方案是加入稍过量的碳;固体产物中可能含有少量Na2SO3,设计实验为取少量反应后的固体于试管中,加蒸馏水溶解,滴加适量稀盐酸,若出现淡黄色沉淀,则固体中含亚硫酸钠,反之不含;
(4)经实验测定,硫酸钠与炭粉在一定条件下反应还可生成等物质的量的两种盐和体积比为1:3的CO2和CO两种气体,C失去电子,S得到电子,若CO2和CO分别为1mol、3mol,失去电子为10mol,则S得到10mol电子,应生成等量的Na2S、Na2SO3,反应方程式为2Na2SO4+4C![]() Na2S+Na2SO3+3CO↑+CO2↑。
Na2S+Na2SO3+3CO↑+CO2↑。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案【题目】下表是周期表的一部分,根据A~I在周期表中的位置,回答以下问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | A | |||||||
2 | D | E | G | |||||
3 | B | C | J | F | H | I |
(1)表中元素,化学性质最不活泼的是__(用元素符号表示,本小题下同);被选做相对原子质量标准的核素是__(填核素符号);除稀有气体外,原子半径最大的是__,可用于制半导体材料的元素是__,形成化合物中种类最多的元素是__。
(2)最高价氧化物的水化物酸性最强的是__(填化学式),A分别与D、E、F、G、H形成的化合物中,最稳定的是__(填化学式)。
(3)B和H形成化合物的电子式为_。
(4)元素E和元素H的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式__。
(5)B、C两元素的最高价氧化物对应水化物之间反应的离子方程式是__。