题目内容
已知:硫酸铜溶液中滴入氨基乙酸钠(H2N—CH2—COONa)即可得到配合物A。其结构如右图:
(1)Cu元素基态原子的外围电子排布式为 。
(2)1mol氨基乙酸钠中含有σ键的数目为 。
(3)氨基乙酸钠分解产物之一为二氧化碳,写出二氧化碳的一种等电子体 (写化学式)。已知二氧化碳在水中溶解度不大,却易溶于二硫化碳,请解释原因 。
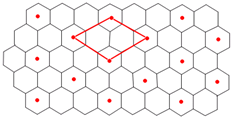
(4)硫酸根离子的空间构型为 ;已知:硫酸铜灼烧可以生成一种红色晶体,其结构如右图,则该化合物的化学式是 。

(1)Cu元素基态原子的外围电子排布式为 。
(2)1mol氨基乙酸钠中含有σ键的数目为 。
(3)氨基乙酸钠分解产物之一为二氧化碳,写出二氧化碳的一种等电子体 (写化学式)。已知二氧化碳在水中溶解度不大,却易溶于二硫化碳,请解释原因 。
(4)硫酸根离子的空间构型为 ;已知:硫酸铜灼烧可以生成一种红色晶体,其结构如右图,则该化合物的化学式是 。

(1)3d104s1
(2)8NA
(3)N2O(或SCN?、N3?等)
二氧化碳与二硫化碳均是非极性分子,而水是极性分子,依据相似相容原理,所以二氧化碳在水中溶解度不大,却易溶于二硫化碳
(4)正四面体型 Cu2O
(2)8NA
(3)N2O(或SCN?、N3?等)
二氧化碳与二硫化碳均是非极性分子,而水是极性分子,依据相似相容原理,所以二氧化碳在水中溶解度不大,却易溶于二硫化碳
(4)正四面体型 Cu2O
(1)Cu是29号元素,其基态时外围电子排布式是3d104s1;
(2)根据氨基乙酸钠的结构简式可知,1mol氨基乙酸钠中含有σ键数为8NA;
(3)根据等电子原理,二氧化碳与N2O、SCN-、N3-为等电子体;二氧化碳在水中溶解度不大,却易溶于二硫化碳,其原因是二氧化碳与二硫化碳都是非极性分子,而水分子是极性分子,所以根据相似相溶原理,二氧化碳在水中溶解度不大,在二硫化碳中溶解度大;
(4)硫酸根离子是AB4型,即为正四面体;由图可以判断,1个晶胞中含有4个Cu和2个O,即分子式为Cu2O。
(2)根据氨基乙酸钠的结构简式可知,1mol氨基乙酸钠中含有σ键数为8NA;
(3)根据等电子原理,二氧化碳与N2O、SCN-、N3-为等电子体;二氧化碳在水中溶解度不大,却易溶于二硫化碳,其原因是二氧化碳与二硫化碳都是非极性分子,而水分子是极性分子,所以根据相似相溶原理,二氧化碳在水中溶解度不大,在二硫化碳中溶解度大;
(4)硫酸根离子是AB4型,即为正四面体;由图可以判断,1个晶胞中含有4个Cu和2个O,即分子式为Cu2O。

练习册系列答案
相关题目
 键:
键:
 是钴的一种配合物,易溶于水,与钾离子反应生成淡黄色的
是钴的一种配合物,易溶于水,与钾离子反应生成淡黄色的 沉淀,可用于检验K+的存在。
沉淀,可用于检验K+的存在。 的价层电子排布图为_____
的价层电子排布图为_____