题目内容
【题目】某二元化合物X是锂硫电池的电极材料,为探究其组成进行了如下实验:
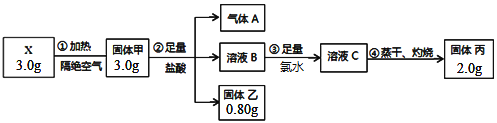
固体乙是一种单质,固体丙呈红棕色,将气体A通入溶液C中也能生成固体乙。
请回答:
(1)X的化学式是_________________,步骤①的化学方程式是_________________________。
(2)气体A通入溶液C发生反应的离子方程式是_________________________。
【答案】FeS2FeS2![]() FeS+SH2S+2Fe3+=S↓+2Fe2++2H+
FeS+SH2S+2Fe3+=S↓+2Fe2++2H+
【解析】
溶液B中加入足量氯水,得到溶液C,溶液C蒸干、灼烧得到固体丙,固体丙呈红棕色,则丙为氧化铁,说明溶液B中含有亚铁离子,溶液C中含有铁离子;固体乙是一种单质,将气体A通入溶液C(FeCl3)中也能生成固体乙,根据题意,气体A为硫化氢,固体乙为硫单质;说明X中含有铁和硫元素,故固体甲为硫化亚铁(FeS),氧化铁的质量为2g,物质的量为![]() =
=![]() mol,含有铁元素的质量为
mol,含有铁元素的质量为![]() mol×2×56g/mol=1.4g,则X中含有硫元素1.6g,X中铁元素与硫元素的物质的量之比=
mol×2×56g/mol=1.4g,则X中含有硫元素1.6g,X中铁元素与硫元素的物质的量之比=![]() =
=![]() ,则X的化学式为FeS2。
,则X的化学式为FeS2。
(1)根据上述分析,X为FeS2,步骤①中FeS2分解生成硫化亚铁和硫,反应的化学方程式为FeS2![]() FeS+S,故答案为:FeS2;FeS2
FeS+S,故答案为:FeS2;FeS2![]() FeS+S;
FeS+S;
(2)气体A(H2S)通入溶液C(FeCl3)中发生反应的离子方程式为H2S+2Fe3+=S↓+2Fe2++2H+,故答案为:H2S+2Fe3+=S↓+2Fe2++2H+。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案【题目】粉煤灰(主要含有 SiO2、Fe2O3、Al2O3 等)是燃煤发电过程中产生的废渣,粉煤灰的综合利用具有 很大的价值。
Ⅰ.研究人员通过实验对粉煤灰中铝和铁元素的分离工艺进行了研究。
(1)以硫酸溶液分解粉煤灰,使其中的铝、铁元素溶出,过滤实现初步分离。
①写出硫酸溶液与 Fe2O3 反应的离子方程式_____。
②初步分离得到的滤渣主要成分是_____。
(2)向(1)分离所得的滤液中加入还原剂使 Fe3+转化为 Fe2+,结合下表分析其原因____。
物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
沉淀区间(pH) | 7.06~8.95 | 1.94~3.20 | 3.69~4.8 |
(3)使用碱性较弱的氨水为pH调节剂,进行分离实验。
①氨水使滤液中铝离子沉淀的离子方程式为_____。
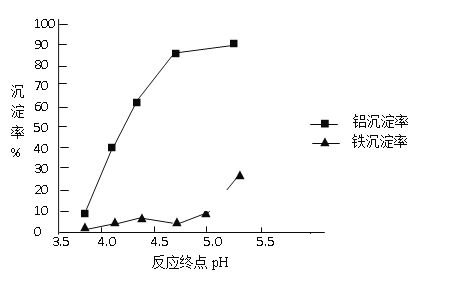
②反应终点的pH对铝和铁分离效果的影响如下图。根据实验结果,为达到好的分离效果,反应过程中控制pH的 范围是______________,选择该范围的理由是___________________。
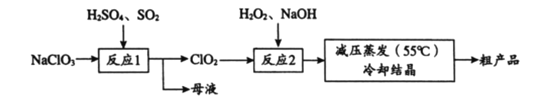
Ⅱ.NH4HSO4和H2SO4按物质的量比1∶1混合配制成浸取液,220℃时,可将高铝粉煤灰中Al2O3转化为硫酸铝铵 [NH4Al(SO4)2],然后分离、煅烧获得纯Al2O3。 已知硫酸铝铵:①溶解度:0℃时,S=5.2g;100℃时,S=421.9g。②280℃时分解。
(1)依据资料可知,将硫酸铝铵与其他溶质分离的方法是_____。
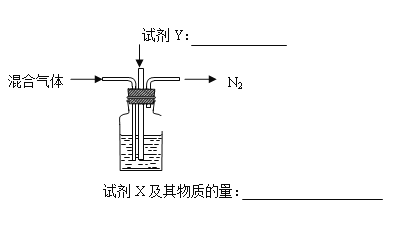
(2)煅烧 NH4Al(SO4)2 同时得到混合气体(NH3、N2、SO2、SO3、H2O)。若 16 mol 混合气体按如下装置被完全吸收制得浸取液,请将下图中试剂(化学式)及其物质的量补充完整。____________,___________
4NH4Al(SO4)2 ![]() 2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑
2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑