题目内容
19.下列装置示意图中的实验不能达到目的是( )| A. | 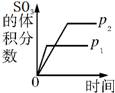 研究压强对反应的影响(p2>p1) | |
| B. |  研究温度对反应的影响 | |
| C. | 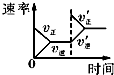 研究平衡体系中增加O2浓度对反应的影响 | |
| D. | 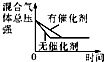 体积恒定的密闭容器中催化剂对反应的影响 |
分析 A、合成三氧化硫反应是气体体积缩小的反应,则利用压强对化学平衡及化学反应速率的影响,然后结合图象来分析;
B、合成三氧化硫的反应是放热反应,利用温度对化学平衡的影响及图象来分析;
C、利用增大反应物的浓度对化学平衡移动的影响并结合图象来分析;
D、利用催化剂对化学反应速率及化学平衡的影响,结合图象来分析.
解答 解:A、该反应中增大压强平衡向正反应方向移动,则三氧化硫的体积分数增大,并且压强越大,化学反应速率越大,达到化学平衡的时间越少,与图象不符,故A错误;
B、因该反应是放热反应,升高温度化学平衡向逆反应反应移动,则氧气的转化率降低,与图象中转化率增大不符,故B错误;
C、反应平衡后,增大氧气的量,则这一瞬间正反应速率增大,逆反应速率不变,然后正反应速率在不断减小,逆反应速率不断增大,直到新的平衡,与图象符合,故C正确;
D、因催化剂对化学平衡无影响,但催化剂加快化学反应速率,则有催化剂时达到化学平衡的时间少,与图象不符,故D错误;
故选C.
点评 本题考查化学平衡与图象,明确影响化学反应速率及化学平衡的影响因素,图象中纵横坐标的含义即可解答.

练习册系列答案
相关题目
9.下列物质对应关系正确的是( )
| A. | 淀粉检验方法:加碘化钾变蓝 | B. | 蛋白质检验方法:浓硝酸或燃烧法 | ||
| C. | 蛋白质最终水解产物:葡萄糖 | D. | 淀粉最终水解产物:二氧化碳 |
4. (1)25℃时,下列4种溶液.请回答下列问题.
(1)25℃时,下列4种溶液.请回答下列问题.
A.0.01 mol•L-1 氨水 B.0.01mol•L-1 NaOH 溶液
C.pH=2的CH3COOH溶液 D.pH=2的HCl溶液
①上述4种溶液中,水的电离程度最大的是A(填序号);
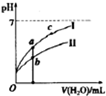
②若将C、D溶液分別稀释10倍,pH变化如图,判断曲线I对应的溶液为D(填序号),图中a、b、c三点对应溶液的导电能力由强到弱的顺序是b>a>c.(用a、b、c 表示)
③若将B、C溶液等体积混合,所得溶液的pH<7(填“>”、“<”或“=”).
(2)已知25℃:
①一元酸H3PO2:的电离方程式为H3PO2?H2PO2-+H+;
②H2S溶液与NaA溶液反应的化学方程式为H2S+NaA=NaHS+HA;
③经测定,25℃时,0.01 mol•L-1 Na2S溶液的PH为11,则:
c(H+)+c(HS-)+2c(H2S)=1.0×10-3mol/L.
 (1)25℃时,下列4种溶液.请回答下列问题.
(1)25℃时,下列4种溶液.请回答下列问题.A.0.01 mol•L-1 氨水 B.0.01mol•L-1 NaOH 溶液
C.pH=2的CH3COOH溶液 D.pH=2的HCl溶液
①上述4种溶液中,水的电离程度最大的是A(填序号);
②若将C、D溶液分別稀释10倍,pH变化如图,判断曲线I对应的溶液为D(填序号),图中a、b、c三点对应溶液的导电能力由强到弱的顺序是b>a>c.(用a、b、c 表示)
③若将B、C溶液等体积混合,所得溶液的pH<7(填“>”、“<”或“=”).
(2)已知25℃:
| 物质 | H3PO2 | H2S | 一元酸HA |
| Kn | Kn=5.9×l0-2 | Kn1=9.1×l0-8 Kn2=l.l×l0-12 | Kn=l.1×1O-10 |
②H2S溶液与NaA溶液反应的化学方程式为H2S+NaA=NaHS+HA;
③经测定,25℃时,0.01 mol•L-1 Na2S溶液的PH为11,则:
c(H+)+c(HS-)+2c(H2S)=1.0×10-3mol/L.
11.下列说法正确的是( )
| A. | s能级原子轨道呈球形,其电子运动轨迹呈球形 | |
| B. | P能级轨道数随电子层数递增而增多 | |
| C. | 在基态多电子原子中,N层上的电子能最一定比M层上的高 | |
| D. | 在基态多电子原子中,不可能有两个运动状态完全相同的电子 |
5.随着化石能源的日益减少,能源危机成为目前人类面临的重要问题.主要利用化学方法产生新能源的事例为( )
| A. | 风力发电 | B. | 潮汐能发电 | ||
| C. | 水力发电 | D. | 太阳能光解水制取H2 |
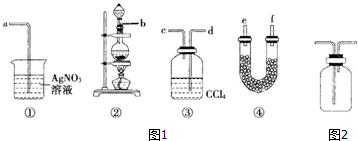

 实验室用如图装置,利用Cu与HNO3反应来制取NO并用排水法收集气体.
实验室用如图装置,利用Cu与HNO3反应来制取NO并用排水法收集气体.