题目内容
X、Y、Z、W为原子序数依次增大的短周期元素。其形成的小分子化合物Y2X2、Z2X4、X2W2中,相应分子内各原子最外层电子都满足稳定结构.下列说法正确的是
A. X、Y、Z、W的原子半径的大小关系为:W>Y>Z>X
B. 在化合物Y2X2、Z2X4、X2W2的一个分子中,所含的共用电子对数相等
C. X、Y、Z、W四种元素可形成化学式为X7Y2ZW2的有机物
D. 与元素Y、Z相比,元素W形成的简单氢化物最稳定,是因为其分子间存在氢键
练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
11.不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,不一定能产生沉淀的是( )
| 序号 | 甲 | 乙 | 丙 |
| A | CO2 | SO2 | 澄清石灰水 |
| B | HCl | CO2 | Ba(OH)2 |
| C | CO2 | SO2 | Ba(NO3)2 |
| D | CO2 | NH3 | CaCl2 |
| A. | A | B. | B | C. | C | D. | D |


 Fe(OH)3 + 3 H+,下列操作能使FeCl3的水解程度增大且溶液的酸性增强的是( )
Fe(OH)3 + 3 H+,下列操作能使FeCl3的水解程度增大且溶液的酸性增强的是( )

 2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
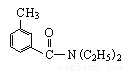 ;DEET在一定条件下,可通过下面的路线来合成:
;DEET在一定条件下,可通过下面的路线来合成: