题目内容
【题目】下列说法正确的是
A. 相同体积、相同浓度的氨水和NaOH溶液中和盐酸的能力相同
B. 醋酸溶液中只存在一个电离平衡体系
C. 0.1mol · L-1的氨水能使酚酞试液变红,说明氨水是弱电解质水溶液
D. 同浓度同体积的醋酸和盐酸分别与足量镁反应时,放出H2的速率相同
【答案】A
【解析】相同体积、相同浓度的氨水和NaOH溶液说明二者的物质的量相同,故中和盐酸的能力相同,A项正确;醋酸溶液中只存在两个电离平衡体系:CH3COOH![]() CH3COO—+H+、H2O
CH3COO—+H+、H2O![]() OH—+H+,B项错误;碱溶液均能使酚酞试液变红,C项错误;盐酸为强电解质,完全电离,醋酸为弱电解质,部分电离,同浓度同体积的醋酸和盐酸,开始时,盐酸中
OH—+H+,B项错误;碱溶液均能使酚酞试液变红,C项错误;盐酸为强电解质,完全电离,醋酸为弱电解质,部分电离,同浓度同体积的醋酸和盐酸,开始时,盐酸中![]() ,与镁反应速率快,放出氢气的速率快,D项错误。
,与镁反应速率快,放出氢气的速率快,D项错误。

【题目】某校化学课外研究小组为研究浓硫酸与金属M 反应的气体生成物,进行了下列实验活动:
【提出假设】
假设1:气体生成物只有SO2;
假设2:气体生成物只有H2;
假设3:_______________________________________。
【实验验证】实验装置及实验中使用的试剂如图:
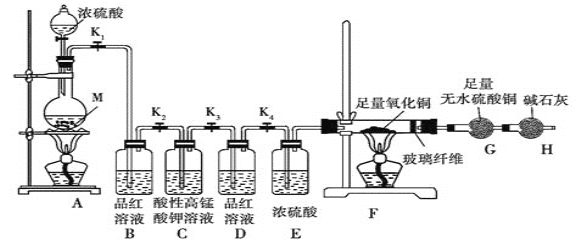
在装入药品前,甲同学检查装置A 的气密性,方法是________________________________________。
(2)乙同学通过所学知识排除了上面提出的一个假设,他排除的是假设_____,理由是______________________________________________________。
(3)如果假设3 正确,填写下表中的实验现象:
装置 | B | F | G |
实验现象 | _____ | _____ | _____ |
装置C 的作用是___________________________,写出装置C中发生反应的离子方程式__________________________________________________。
(5)装置D 的作用是________________________________________。