题目内容
常温下,如果要使100mL pH=12的NaOH溶液的pH变为11:
(1)若加水稀释,则应加入 mL.
(2)若加pH=10的NaOH溶液,则应加入 mL.
(3)若加pH=2的HCl溶液,则应加入 mL.
(4)若加0.01mol?L-1的H2SO4溶液,则应加入 mL.
(1)若加水稀释,则应加入
(2)若加pH=10的NaOH溶液,则应加入
(3)若加pH=2的HCl溶液,则应加入
(4)若加0.01mol?L-1的H2SO4溶液,则应加入
考点:pH的简单计算
专题:计算题,电离平衡与溶液的pH专题
分析:(1)先根据溶液的pH计算氢氧根离子浓度,再根据c1V1=c2(V1+V2)计算加入的水体积;
(2)先根据溶液的pH计算氢氧根离子浓度,再根据c1V1+c2V2=c3(V1+V2)计算加入的氢氧化钠溶液体积;
(3)先计算混合溶液中氢氧根离子浓度,再根据c(OH-)=
进行计算;
(4)先计算混合溶液中氢氧根离子浓度,再根据c(OH-)=
进行解答即可.
(2)先根据溶液的pH计算氢氧根离子浓度,再根据c1V1+c2V2=c3(V1+V2)计算加入的氢氧化钠溶液体积;
(3)先计算混合溶液中氢氧根离子浓度,再根据c(OH-)=
| n(碱)-n(酸) |
| V(酸)+V(碱) |
(4)先计算混合溶液中氢氧根离子浓度,再根据c(OH-)=
| n(OH-)-n(H+) |
| V(酸)+V(碱) |
解答:
解:(1)pH=12 的NaOH溶液中氢氧根离子浓度为0.01mol/L,pH=11的氢氧化钠溶液中氢氧根离子浓度是0.001mol/L,设加入水的体积是V2,c1V1=c2(V1+V2)=0.01mol/L×0.1L=(0.1+V2)L,V2=
=0.9L=900mL,
故答案为:900;
(2)pH=12 的NaOH溶液中氢氧根离子浓度是0.01mol/L,pH=11的氢氧化钠溶液中氢氧根离子浓度是0.001mol/L,pH=10的氢氧化钠溶液中氢氧根离子浓度是0.0001mol/L,
设加入pH=10的NaOH溶液体积是V2,
c1V1+c2V2=c3(V1+V2)=0.01mol/L×0.1L+0.0001mol/L×V2=0.001mol/L(0.1+V2),
V2=1L=1000mL,
故答案为:1000;
(3)pH=2的HCl溶液中氢离子浓度是0.01mol/L,设加入盐酸的体积是V,
c(OH-)=
=
=0.001mol/L,
解得:V=81.8mL,
故答案为:81.8;
(4)0.01mol?L-1的H2SO4溶液中氢离子浓度为0.02mol/L,设加入硫酸的体积为V,
c(OH-)=
=0.001mol/L,
解得:V=42.86mL,
故答案为:42.86.
| 0.01mol/L×0.1L |
| 0.001mol/L |
故答案为:900;
(2)pH=12 的NaOH溶液中氢氧根离子浓度是0.01mol/L,pH=11的氢氧化钠溶液中氢氧根离子浓度是0.001mol/L,pH=10的氢氧化钠溶液中氢氧根离子浓度是0.0001mol/L,
设加入pH=10的NaOH溶液体积是V2,
c1V1+c2V2=c3(V1+V2)=0.01mol/L×0.1L+0.0001mol/L×V2=0.001mol/L(0.1+V2),
V2=1L=1000mL,
故答案为:1000;
(3)pH=2的HCl溶液中氢离子浓度是0.01mol/L,设加入盐酸的体积是V,
c(OH-)=
| n(碱)-n(酸) |
| V(酸)+V(碱) |
| 0.01mol/L×(0.1-V)L |
| (0.1+V)L |
解得:V=81.8mL,
故答案为:81.8;
(4)0.01mol?L-1的H2SO4溶液中氢离子浓度为0.02mol/L,设加入硫酸的体积为V,
c(OH-)=
| 0.01mol/L×0.1L-0.02mol/L×V |
| 0.1L+V |
解得:V=42.86mL,
故答案为:42.86.
点评:本题考查溶液pH的简单计算,题目难度中等,注意掌握溶液酸碱性与溶液pH的计算方法,明确酸碱中和反应实质为解答本题的关键,试题培养了学生的化学计算能力.

练习册系列答案
 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案
相关题目
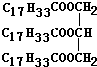 +3H2
+3H2