题目内容
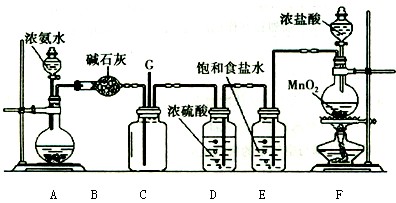
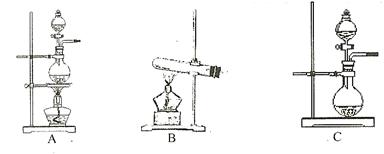
(9分)拟用下图装置制取表中的四种干燥、纯净的气体(图中铁架台、铁夹、加热及气体收集装置均已略去;必要时可以加热;a、b、c、d表示相应仪器中加入的试剂).
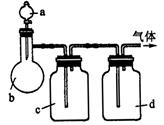
(1)上述方法中可以得到干燥、纯净的气体是____________.
(2)指出不能用上述方法制取的气体,并说明理由(可以不填满)
①气体____________,理由是____________.
②气体____________,理由是____________.
③气体____________,理由是____________.
④气体____________,理由是____________.

| 气体 | a | b | c | d |
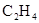 | 乙醇 | 浓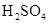 | 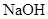 溶液 溶液 | 浓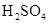 |
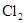 | 浓盐酸 | 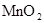 | 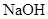 溶液 溶液 | 浓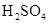 |
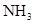 | 饱和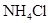 溶液 溶液 | 消石灰 | 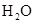 | 固体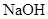 |
| NO | 稀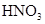 | 铜屑 | 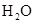 | 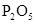 |
(1)上述方法中可以得到干燥、纯净的气体是____________.
(2)指出不能用上述方法制取的气体,并说明理由(可以不填满)
①气体____________,理由是____________.
②气体____________,理由是____________.
③气体____________,理由是____________.
④气体____________,理由是____________.
(1)NO (2)①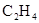 装置中没有温度计,无法控制反应温度
装置中没有温度计,无法控制反应温度
②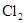 反应生成的
反应生成的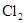 被C中的NaOH溶液吸收了.
被C中的NaOH溶液吸收了.
③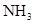 反应生成的
反应生成的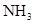 被C中的
被C中的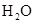 吸收了
吸收了
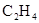 装置中没有温度计,无法控制反应温度
装置中没有温度计,无法控制反应温度②
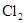 反应生成的
反应生成的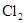 被C中的NaOH溶液吸收了.
被C中的NaOH溶液吸收了.③
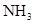 反应生成的
反应生成的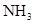 被C中的
被C中的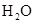 吸收了
吸收了(1)制取乙烯需要温度计控制温度170℃,所以根据装置图可判断,不能制得纯净的乙烯;氯气能被氢氧化钠溶液吸收,所以无法收集到氯气;氨气极易溶于水,如果用水,则生成的氨气被是完全吸收,得不到氨气,所以只能制取的是NO。

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目

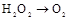
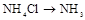
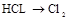
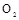 的装置制备
的装置制备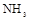 ,应选择的试剂为 .
,应选择的试剂为 .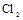 需用
需用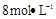 的盐酸1OOml,现用
的盐酸1OOml,现用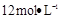 的盐酸来配制。
的盐酸来配制。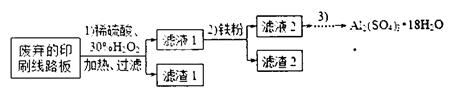
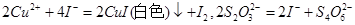
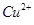 含量将会 (填“偏高”、“偏
含量将会 (填“偏高”、“偏
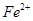 除去。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mo1.L-1计算)。
除去。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mo1.L-1计算)。