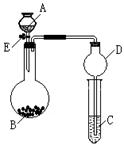
题目内容
(20分)下面是用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的稀H2SO4 500ml的操作,请按要求填空:
(1)所需浓H2SO4的体积为
(2)如果实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好。量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将 (偏高、偏低、无影响)。
(3)将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100mL水的 里,并不断搅拌,目的是 。
(4)将 的上述溶液沿 注入 中,并用50mL蒸馏水洗涤烧杯2~3次,洗涤液要 中,并摇匀。
(5)加水至距刻度 处,改用 加水,使溶液的凹液面正好跟刻度相平。
(1)所需浓H2SO4的体积为
(2)如果实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好。量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将 (偏高、偏低、无影响)。
(3)将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100mL水的 里,并不断搅拌,目的是 。
(4)将 的上述溶液沿 注入 中,并用50mL蒸馏水洗涤烧杯2~3次,洗涤液要 中,并摇匀。
(5)加水至距刻度 处,改用 加水,使溶液的凹液面正好跟刻度相平。
.14ml;15ml;偏低;烧杯;防止浓硫酸飞溅;冷却后;玻璃棒;500ml容量瓶;转移到容量瓶;1-2cm;胶头滴管
考查一定物质的量浓度的配制。
(1)根据稀释过程中溶质不变可知,0.5×0.5=1.84V×98%÷98,解得V=14ml即浓硫酸的体积是14ml。
(2)规格越接近,误差越小,所以应该选择15ml的量筒。水洗后直接量取,相当于稀释,浓度偏低。
(3)由于浓硫酸的密度大于水的,且溶于水放出大量的热,所以浓硫酸的稀释应该在烧杯中完成,且需要不断的搅拌,以防止浓硫酸飞溅。
(4)转移之前,需要冷却,转移时用玻璃棒引流,注入500ml容量瓶中。烧杯和玻璃棒都需要洗涤,且洗涤液要注入容量瓶中。
(5)当接近刻度线1~2cm时,用胶头滴管加水定容。
(1)根据稀释过程中溶质不变可知,0.5×0.5=1.84V×98%÷98,解得V=14ml即浓硫酸的体积是14ml。
(2)规格越接近,误差越小,所以应该选择15ml的量筒。水洗后直接量取,相当于稀释,浓度偏低。
(3)由于浓硫酸的密度大于水的,且溶于水放出大量的热,所以浓硫酸的稀释应该在烧杯中完成,且需要不断的搅拌,以防止浓硫酸飞溅。
(4)转移之前,需要冷却,转移时用玻璃棒引流,注入500ml容量瓶中。烧杯和玻璃棒都需要洗涤,且洗涤液要注入容量瓶中。
(5)当接近刻度线1~2cm时,用胶头滴管加水定容。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
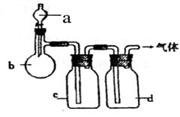
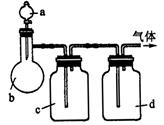
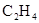
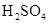
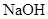 溶液
溶液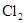
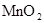
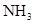
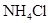 溶液
溶液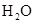
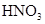
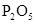
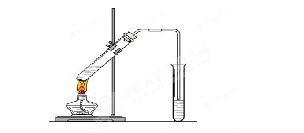
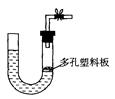

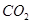 发生装置(X)的气密性,请写出主要操作过程:
发生装置(X)的气密性,请写出主要操作过程: