题目内容
在盛有AgNO3、HCl、Na2CO3、CaCl2、NaI五种无色溶液的试剂瓶上,分别贴有①~⑤的编号。将它们两两混合,产生的现象如右表所列(其中“↑”表示产生气体,“↓”表示生成沉淀,“—”表示无现象):

(1)写出③、④、⑤三种物质的化学式为: ③ 、④ 、⑤ 。
(2)写出下列反应的离子方程式:①+② 。

(1)写出③、④、⑤三种物质的化学式为: ③ 、④ 、⑤ 。
(2)写出下列反应的离子方程式:①+② 。
(1)CaCl2 AgNO3 NaI
(2)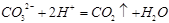
(2)
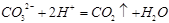
试题分析:(1)观察五种物质可知,只有HCl、Na2CO3混合才会生成气体,则①②为这两种,其他三种物质,只有AgNO3与所有物质混合都有沉淀产生,即为④;而NaI只与AgNO3才能反应,故为⑤;那么③只能是CaCl2;再根据HCl 、Na2CO3与③、④、⑤的反应现象,则可判断①为Na2CO3,②为HCl。
(2)HCl 、Na2CO3均为强电解质,全拆,Na+ 和Cl-实际没有参加反应。
点评:利用物质两两混合的现象推断各物质分别是什么,是高考常见的考查题型。考生在备考中应注意积累常见物质的反应及现象。

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目


 乙
乙 丙。下列有关物质的推断不正确的是( )
丙。下列有关物质的推断不正确的是( )
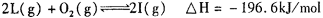 。向一个容积不变的 容器中,充入2mol L和1molO2,使之充分反应,放出的热量为Q,则Q_______196. 6kJ (填“ >”、“〈”或“=”)。
。向一个容积不变的 容器中,充入2mol L和1molO2,使之充分反应,放出的热量为Q,则Q_______196. 6kJ (填“ >”、“〈”或“=”)。
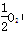 (g)===FeO(s) ΔH=-272.0 kJ·mol-1
(g)===FeO(s) ΔH=-272.0 kJ·mol-1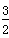 O2(g)===X2O3(s) ΔH=-1 675.7 kJ·mol-1
O2(g)===X2O3(s) ΔH=-1 675.7 kJ·mol-1