题目内容
A、B、C、D、E为原子序数依次增大的五种短周期主族元素。其中B原子最外层电子数是次外层的3倍。A、C与B相邻,D最外层只有1个电子,E单质既能与强酸反应,又能与强碱反应。下列比较正确的是( )
A.最高正价:C>E>A B.气态氢化物稳定性:C>B>A
C.原子半径:B>D>A D.原子失电子能力:D>C>E
A.最高正价:C>E>A B.气态氢化物稳定性:C>B>A
C.原子半径:B>D>A D.原子失电子能力:D>C>E
B
首先短周期主族元素为前三周期元素,原子核外不超过三层电子;其中B原子最外层电子数是次外层的3倍,知B原子最多有两个电子层且最外层有6个电子,从而推出B原子是8号元素氧;A、C与B相邻,知A为氮,C为氟,又据E单质既能与强酸反应,又能与强碱反应知E原子是典型的两性元素铝元素的原子,D原子序数介于9与13之间且D最外层只有1个电子那它应该是第一主族元素钠,上述分析知:
答案A错误,C不表现正价
B 正确 按CA即氟、氧、氮的顺序元素非金属性逐渐减弱其气态氢化物稳定性也逐渐减弱
C 错误,氧 氮同周期,据周期律氧原子半径应小于氮原子半径
D错误 原子失电子能力取决于元素的金属性而其中C即氮原子是典型的非金属元素的原子只有的电子能力。
答案A错误,C不表现正价
B 正确 按CA即氟、氧、氮的顺序元素非金属性逐渐减弱其气态氢化物稳定性也逐渐减弱
C 错误,氧 氮同周期,据周期律氧原子半径应小于氮原子半径
D错误 原子失电子能力取决于元素的金属性而其中C即氮原子是典型的非金属元素的原子只有的电子能力。

练习册系列答案
相关题目
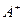 比
比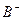 少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1。请回答下列问题:
少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1。请回答下列问题: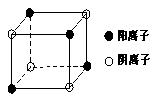
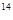 C含量,能测出古代物品所处的年代。
C含量,能测出古代物品所处的年代。