题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,11.2 L四氯化碳中含有的分子数0.5NA
B.常温常压下,18.0 g水所含的电子数为10 NA
C.300mL 0.1mol/L的NaCl的溶液含有0.03NA个NaCl分子
D.1.2 g熔融的NaHSO4含有阴阳离子总数为0.03NA
【答案】B
【解析】
A. 标况下四氯化碳为液体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B. 18.0g水的物质的量为1mol,而一个水分子中含10个电子,故1mol水中含电子为10NA个,故B正确;
C. 氯化钠是离子化合物,且溶于水后完全电离,故在氯化钠溶液中无氯化钠分子,故C错误;
D. 1.2g硫酸氢钠的物质的量为n=![]() =0.01mol,而硫酸氢钠在熔融时只能电离为钠离子和硫酸氢根离子,故0.01mol熔融的硫酸氢钠中含离子为0.02NA个,故D错误。
=0.01mol,而硫酸氢钠在熔融时只能电离为钠离子和硫酸氢根离子,故0.01mol熔融的硫酸氢钠中含离子为0.02NA个,故D错误。
故选:B。

 名校课堂系列答案
名校课堂系列答案【题目】为探究Na与CO2反应的产物,某化学兴趣小组按如图所示装置进行实验。
己知:CO+2Ag(NH3)2OH=2Ag↓+ (NH4)2CO3+2NH3
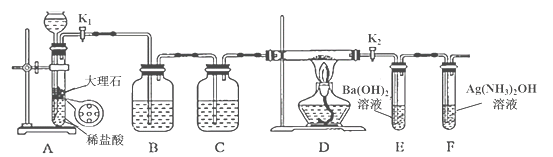
回答下列问题:
(1)B中的溶液为______________。
(2)先称量硬质玻璃管的质量为ml g,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是m2 g。再进行下列实验操作,其正确顺序是____________(填标号);重复上述操作步骤,直至硬质玻璃管恒重,称得质量为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.称量硬质玻璃管
d.打开K1和K2,通入CO2至E中出现浑浊 e.关闭K1和K2 f.冷却到室温
(3)加热硬质玻璃管一段时间,观察到以下现象:
①钠块表面变暗,熔融成金属小球;
②继续加热,钠迅速燃烧,产生黄色火焰。反应完全后,管中有大量黑色物质;
③F中试管内壁有银白物质产生。
产生上述②现象的原因是____________________________________________________;
(4)探究固体产物中钠元素的存在形式
假设一:只有Na2CO3; 假设二:只有Na2O; 假设三:Na2O和Na2CO3均有;
完成下列实验设计,验证上述假设:
步骤 | 操作和现象 | 结论 |
1 | 将硬质玻璃管中的固体产物溶于水后过滤; | 假设一成立 |
2 | 往步骤1所得滤液中_________________________________; 现象:____________________________________。 |
(5)根据上述实验现象及下表实验数据,写出Na与CO2反应的总化学方程式_____________。
m1 | m2 | m3 |
66.7g | 69.0g | 72.1g |