题目内容
氢化铵(NH4H)与氯化铵的结构相似,又知它与水反应有气体生成。下列关于氢化铵叙述不正确的是( )。
| A.是离子化合物,含有离子键和共价键 |
B.电子式是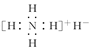 |
| C.与水反应时,是还原剂 |
| D.固体投入少量的水中,有两种气体产生 |
B
解析

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
近年来,科学家合成了一种稳定的氢铝化合物Al2H6。Al2H6的球棍模型如下图所示,它的熔点为150℃,可用作高能燃料或储氢材料。下列说法正确的是 ( )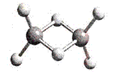
| A.Al2H6可以燃烧,产物为氧化铝和水 |
| B.1mol Al2H6中约含有4.8×1024个σ键 |
| C.60g Al2H6中含铝原子约为1.2×1023个 |
| D.Al2H6在固态时所形成的晶体是离子晶体 |
有关物质结构的下列说法中正确的是
| A.碘升华时破坏了共价键 |
| B.含极性键的共价化合物一定是电解质 |
| C.氯化钠固体中的离子键在溶于水时被破坏 |
| D.HF的分子间作用力大于HCl,故HF比HCl更稳定 |
下列对分子或离子的立体构型判断不正确的是 ( )。
| A.NH4+和CH4都是正四面体形 |
| B.CO2和CS2都是直线形 |
| C.NCl3和BCl3都是三角锥形 |
| D.H2O和H2S都是V形 |
下列各组物质中,都是由极性键构成的极性分子的一组是( )。
| A.CH4 Br2 | B.H2O NH3 |
| C.CCl4 H2S | D.CO2 HCl |
下列对共价键的说法中,不正确的是( )。
| A.共价键是通过形成共用电子对或原子轨道重叠形成的 |
| B.形成共价键的原子之间电负性相同或相差不大 |
| C.一般情况下一个原子有几个不成对电子就会和几个自旋相反的未成对电子成键 |
| D.共价键是通过共用电子对形成的,不属于电性作用 |
已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H—O键形成时放出热量463 kJ,则氢气中1 mol H—H键断裂时吸收热量为( )。
| A.920 kJ | B.557 kJ | C.436 kJ | D.188 kJ |
下列物质中,含共价键的离子化合物是( )。
| A.MgCl2 | B.N2 | C.HCl | D.Na2O2 |
下列关于σ键和π键的理解不正确的是( )
| A.σ键能单独形成,而π键一定不能单独形成 |
| B.σ键可以绕键轴旋转,π键一定不能绕键轴旋转 |
| C.双键中一定有一个σ键、一个π键,三键中一定有一个σ键、两个π键 |
| D.气体单质中一定存在σ键,可能存在π键 |