题目内容
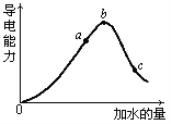
【题目】在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如下图所示,请回答:
(1)写出醋酸的电离方程式___________________________________________。
(2)a、b、c三点溶液中氢离子浓度由小到大的顺序为__________________ 。
(3)a、b、c三点中醋酸的电离程度最大的是_________。
(4)取甲、乙两份等体积c点的溶液,甲用蒸馏水稀释10倍,乙用蒸馏水稀释100倍,则稀释后甲、乙两溶液中的H+浓度:c(H+)甲_____ 10c(H+)乙(填“大于”、“小于”或 “等于”)
【答案】 CH3COOH![]() CH3COO-+H+ c<a<b c 小于
CH3COO-+H+ c<a<b c 小于
【解析】(1)醋酸是弱电解质,在水溶液里只有部分电离,所以醋酸的电离方程式为:CH3COOHCH3COO-+H+,故答案为:CH3COOHCH3COO-+H+;
(2)氢离子浓度越大溶液的导电能力越强,根据图片知,氢离子浓度由小到大的顺序是c<a<b,故答案为:c<a<b;
(3)加入的水越多,溶液越稀,醋酸的电离程度越大,根据图片知,醋酸的电离程度最大是c,故答案为:c;
(4)醋酸是弱电解质,稀释过程中促进醋酸电离,溶液越稀,醋酸的电离程度越大,所以c(H+)甲<10c(H+)乙,故答案为:小于。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目