题目内容
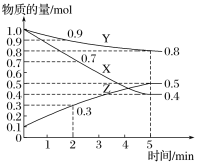
【题目】一定温度下,向容积为2 L的密闭容器中通入气体X、Y、Z,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是
A. 该反应的化学方程式为2X+Y![]() 2Z
2Z
B. 反应开始至2min时,Z的平均反应速率为0.1 mol·L-1·min-1
C. 该反应为可逆反应
D. 4min时,X、Z的速率相等
【答案】C
【解析】
5min时,Y的物质的量减小0.2mol;X的物质的量减小0.6mol;Z的物质的量增加0.4mol;所以Y、X为反应物,Z为生成物;物质的量变化之比等于化学计量系数之比,所以:设X、Y、Z的计量系数分别为a、 b、 c;则a:b:c=0.6:0.2:0.4=3:1:2;所以反应方程式为3X+Y![]() 2Z;
2Z;
A. 综合以上分析可知,该反应的化学方程式为3X+Y![]() 2Z ,A错误;
2Z ,A错误;
B. 反应开始至2min时,Z变化了0.2mol,Z的平均反应速率为0.2/(2×2)= 0.05 mol·L-1·min-1;B错误;
C. 反应进行到5min以后,反应物的量不再发生变化,有剩余,反应没有进行到底,属于可逆反应,C正确;
D. 从图像可知,4min时,X、Z变化的量不相等,所以X、Z的速率不相等,D错误;
综上所述,本题选C。

 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案【题目】乙二酸(HOOC—COOH)俗名草酸,是一种有还原性的有机弱酸,在化学上有广泛应用。
(1)小刚在做“研究温度对化学反应速率的影响”实验时,他往A、B两支试管中均加入4 mL 0.01 mol·L-1的酸性KMnO4溶液和2 mL 0.1 mol·L-1 H2C2O4(乙二酸)溶液,振荡,A试管置于热水中,B试管置于冷水中,记录溶液褪色所需的时间。褪色所需时间tA________tB(填“>”“=”或“<”)。已知该反应的离子方程式:2MnO![]() +5H2C2O4+6H+===10CO2↑+2Mn2++8H2O
+5H2C2O4+6H+===10CO2↑+2Mn2++8H2O
(2)实验室有一瓶混有泥沙的乙二酸样品,小刚利用上述反应的原理来测定其含量,具体操作为:
①配制250 mL溶液:准确称量5.000 g乙二酸样品,配成250 mL溶液。
②滴定:准确量取25.00 mL所配溶液于锥形瓶中,加少量酸酸化,将0.100 0 mol·L-1 KMnO4标准溶液装入______(填“酸式”或“碱式”)滴定管,进行滴定操作。
在滴定过程中发现,刚滴下少量KMnO4标准溶液时,溶液紫红色并没有马上褪去。将锥形瓶摇动一段时间后,紫红色才慢慢消失;再继续滴加时,紫红色就很快褪去,可能的原因是__________________________________________;判断滴定达到终点的现象是________________________________________________________________________。
③计算:重复上述操作2次,记录实验数据如下表。则消耗KMnO4标准溶液的平均体积为________ mL,此样品的纯度为____________。
序号 | 滴定前读数 | 滴定后读数 |
1 | 0.00 | 20.01 |
2 | 1.00 | 20.99 |
3 | 0.00 | 21.10 |
④误差下列操作会导致测定结果偏高的是________。
A.未用KMnO4标准溶液润洗滴定管
B.滴定前锥形瓶内有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.观察读数时,滴定前仰视,滴定后俯视
【题目】某实验小组设计用50 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1氢氧化钠溶液在如图装置中进行中和反应。试回答下列问题:

(1)仪器A的名称__________________________
(2)实验过程中下列操作正确是______________(填字母)。
A.用温度计小心搅拌
B.分多次加入氢氧化钠溶液
C.只进行一次实验,用所获得的数据计算中和热
D.用套在温度计上的A轻轻地上下搅动
(3)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为了计算中和热,某学生实验记录数据如下:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=__________ (结果保留一位小数)。
(4)以下操作,会使测得的中和热ΔH发生怎样的变化?(填“偏大”“偏小”或“不变”)。
①量取稀盐酸时俯视量筒读数,测得的中和热ΔH会_______________ 。
②在中和热测定实验中未用水洗涤温度计上的盐酸直接测定碱的温度,测得的中和热ΔH会_______________。
③若用等浓度的醋酸与 NaOH 溶液反应,则测得的中和热ΔH会 __________,其原因是____________________________________________________________________________。
【题目】用中和滴定法测定某烧碱的纯度。将2.5g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成250mL溶液。根据实验回答下列问题:
(1)滴定
①用____________(仪器)量取20.00mL待测液置于锥形瓶中,再滴加2滴酚酞试液。
②用____________(仪器)盛装0.2000 mol·L-1盐酸标准液,盛装前务必____________,防止标准液浓度降低。
③滴定过程中眼睛应注视_______________,滴定终点的现象为:_______________________________________________________。
(2)有关数据记录如下:
滴定序号 | 待测液体体积(mL) | 滴定前(mL) | 滴定后(mL) | 所消耗盐酸标准液的平均体积(mL) |
1 | 20.00 | 0.50 | 20.70 | V |
2 | 20.00 | 6.00 | 26.00 |
计算V=________ml
(3)纯度计算:NaOH溶液的浓度为________ mol·L-1,烧碱样品的纯度为________。
(4)试判断以下几种情况对烧碱纯度测定的影响(填“偏大”、“偏小”或“无影响”):
①若用蒸馏水冲洗锥形瓶,则会使测定结果________;
②若滴定前滴定管尖嘴有气泡,滴定后气泡消失,则会使测定结果________;
③若刚见到指示剂局部的颜色有变化就停止滴定,则会使测定结果________;
④读数时,若滴定前仰视,滴定后俯视,则会使测定结果________。