��Ŀ����
3�������ǷŴ��ط�����Դ����ҵ����Ҳ���������ã�ij��ѧ��ȤС����ʵ�������÷���������������ͭ�ĺϽ���ȡ��������Һ������ͭ��������죨Fe2O3����ʵ���������£�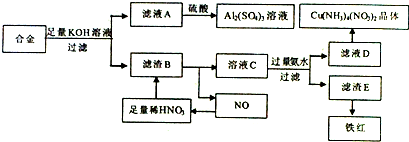
��ش��������⣺
��1��ʵ���ж���õ����˲������ò���ʹ�õ��IJ���������©�����ձ�����������
��2���ںϽ��м���KOH��Һ�������������ӷ�Ӧ����ʽΪ2Al+2OH-+2H2O=2AlO2-+3H2����
��3������ҺA��ֱ�Ӽ�����������õ���������Һ�лẬ������K2SO4�������һ����������ʵ�鷽������ҺA�Ʊ���������������Һ�����������Ʊ�����ͼ������������д���ʵĻ�ѧʽ��

��4����ҺC����������������Fe3+��Cu2+��H+����ҺC������ҺD�е����������ӷ���ʽΪCu2++4NH3•H2O=Cu��NH3��42++4H2O��
��5����ʯī�缫���2L��0.2mol/L KCl��0.2mol/L Cu��NO3��2�Ļ����Һһ��ʱ�����һ�缫������19.2gCu����ʱ��Ҫʹ������Һ�ָ���ԭ���ijɷֺ�Ũ�ȣ�Ӧ��������Һ�м���0.2molCuCl2��0.1molCuO�������ʻ�ѧʽ�Ͷ�Ӧ�����ʵ�������
���� ������������ͭ�ķ����Ͻ�����������������Һ���˵õ�����BΪCu��Fe����ҺΪKAlO2��Һ�������������õ�������������B�м���X����Y����ҺC��Yͨ��������Ӧ����X���ж�XΪHNO3��YΪNO���壬��ҺCΪFe��NO3��3��Cu��NO3��2��������ҺPHʹ�����ӳ����õ�����EΪFe��OH��3����ҺDͨ������Ũ������ȴ�ᾧ������ϴ�ӵõ�����ͭ���壻����E����ϡ�����ܽ�W�����˵õ���ҺFΪ�Ȼ�����ҺF��ͨ������Ũ������ȴ�ᾧ������ϴ�ӵõ��Ȼ������壮
��1�����ݹ��˵�װ�ô��⣻
��2�����ܽ�������������Һ����ƫ����غ�������
��3����ҺA�к�������K2SO4����ҺA�Ʊ���������������Һ����ͨ������������̼��ƫ�������Һ��Ӧ���������������������˵õ���������������ϴ�Ӻ����ϡ����ǡ��ʹ�������������ܽ�õ���������Һ��
��4����ҺCΪFe��NO3��3��Cu��NO3��2�����백ˮ�����γ�ͭ����������Һ��
��5���������Һʱ����������Cu2++2e-=Cu���缫������19.2gCu����֪�����õ�0.6mol���ӣ�����������2Cl--2e-=Cl2����4OH--4e-=O2��+2H2O���������ת�Ƶ�����Ŀ��Ⱥ͵缫����ʽ�Լ�Ԫ���غ���㣮
��� �⣺������������ͭ�ķ����Ͻ�����������������Һ���˵õ�����BΪCu��Fe����ҺΪKAlO2��Һ�������������õ�������������B�м���X����Y����ҺC��Yͨ��������Ӧ����X���ж�XΪHNO3��YΪNO���壬��ҺCΪFe��NO3��3��Cu��NO3��2��������ҺPHʹ�����ӳ����õ�����EΪFe��OH��3����ҺDͨ������Ũ������ȴ�ᾧ������ϴ�ӵõ�����ͭ���壻����E����ϡ�����ܽ�W�����˵õ���ҺFΪ�Ȼ�����ҺF��ͨ������Ũ������ȴ�ᾧ������ϴ�ӵõ��Ȼ������壻
��1�����ݹ��˵�װ�ÿ�֪�����˲����õ��IJ���������©�����ձ�����������
�ʴ�Ϊ��©�����ձ�����������
��2�����ܽ�������������Һ����ƫ����غ���������Ӧ�����ӷ���ʽΪ��2Al+2OH-+2H2O=2AlO2-+3H2����
�ʴ�Ϊ��2Al+2OH-+2H2O=2AlO2-+3H2����
��3��������������ع��������ܺ���ϡ���ᡢ�����ƣ���ҺA�Ʊ���������������Һ����ͨ������������̼��ƫ�������Һ��Ӧ���������������������˵õ���������������ϴ�Ӻ����ϡ����ǡ��ʹ�������������ܽ�õ���������Һ��������ͼ��ʽ�����Ʊ�����ͼΪ�� ��
��
�ʴ�Ϊ��CO2��ϡH2SO4��
��4����ҺCΪFe��NO3��3��Cu��NO3��2����ҺC����������������Fe3+��Cu2+��H+�����백ˮ�����γ�ͭ����������Һ����Ӧ�����ӷ���ʽΪCu2++4NH3•H2O=Cu��NH3��42++4H2O��
�ʴ�Ϊ��Fe3+��Cu2+��H+��Cu2++4NH3•H2O=Cu��NH3��42++4H2O��
��5���������Һʱ����������Cu2++2e-=Cu���缫������19.2gCu����֪�����õ�0.6mol���ӣ�����������2Cl--2e-=Cl2����4OH--4e-=O2��+2H2O����������ȫ����ʱ����Ϊn��Cl-��=0.2��2mol=0.4mol������ת�Ƶ���0.4mol������n��Cl2��=0.2mol����OH-ת�Ƶ���0.2mol����������0.05mol������Ԫ���غ��֪����Ҫʹ������Һ�ָ���ԭ���ijɷֺ�Ũ�ȣ�Ӧ��������Һ�м���0.2molCuCl2��0.1molCuO��
�ʴ�Ϊ��0.2molCuCl2��0.1molCuO��
���� ���⿼�������ʷ����ᴿ�ķ�����������������Ӧ�ã����ջ�����ʵ����������ǹؼ�����Ŀ�Ѷ��еȣ����صļ����DZ����ѵ㣮

 ��ѧ��ʦ����ϵ�д�
��ѧ��ʦ����ϵ�д�| A�� | ������Ϊ67 | B�� | ������Ϊ99 | C�� | ������Ϊ67 | D�� | ������Ϊ67 |
����������������������ʽ����ʱ��pH���£�
| ������ | ��ʼ����ʱ��pH | ��ȫ����ʱ��pH |
| Al��OH��3 | 3.8 | 5.2 |
| Fe��OH��3 | 2.7 | 3.2 |
| Fe��OH��2 | 7.6 | 9.7 |
| Ni��OH��2 | 7.1 | 9.2 |
��2���������ʱ�����������H2SO4���ѧʽ����
��3������H2O2ʱ������Ӧ�����ӷ���ʽΪH2O2+2Fe2++2H+=2Fe3++2H2O��
��4������bΪ������Һ��pH������ΪpH�ĵ��ط�Χ��3.2-7.1��
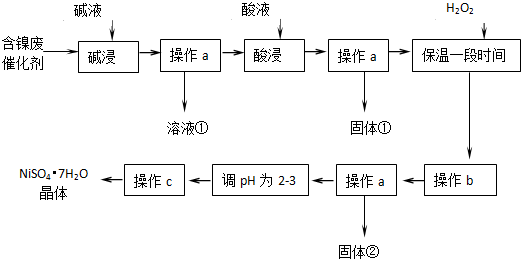
��5��NiS04•7H20�������Ʊ������أ�NiMH����������Ŀǰ�Ѿ���Ϊ��϶���������һ����Ҫ������ͣ�NiMH�е�M��ʾ���������Ͻ𣮸õ���ڳ��������ܷ�Ӧ�Ļ�ѧ����ʽ��Ni��OH��2+M�TNiOOH+MH����NiMH��طŵ�����У������ĵ缫��ӦʽΪNiOOH+H2O+e-=Ni��OH��2+OH-��
| A�� | ��m+n���ض�С��q | B�� | ��m+n���ض�����q | C�� | m�ض�С��q | D�� | m�ض�����q |
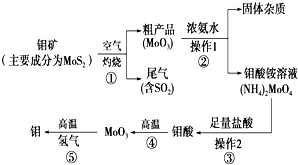
 ����������SiCl4�����ƴ���ķ�Ӧ�У����ÿ����1.12kg����������a kJ������д���÷�Ӧ���Ȼ�ѧ����ʽ��SiCl4��g��+2H2��g��$\frac{\underline{\;1100��\;}}{\;}$Si��s��+4HCl��g������H=+0.025akJ•mol-1��
����������SiCl4�����ƴ���ķ�Ӧ�У����ÿ����1.12kg����������a kJ������д���÷�Ӧ���Ȼ�ѧ����ʽ��SiCl4��g��+2H2��g��$\frac{\underline{\;1100��\;}}{\;}$Si��s��+4HCl��g������H=+0.025akJ•mol-1��

 �к�����ָ�������кͷ�Ӧ����l mol H2O���ų���������ijѧ����ͨ���ⶨ��Ӧ���������ų��������������к��ȣ���50mL0.5mol/L��������50mL0.55mol/L��NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ����ش��������⣺
�к�����ָ�������кͷ�Ӧ����l mol H2O���ų���������ijѧ����ͨ���ⶨ��Ӧ���������ų��������������к��ȣ���50mL0.5mol/L��������50mL0.55mol/L��NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ����ش��������⣺