题目内容
10.放射性同位素钬${\;}_{67}^{166}$Ho,下列有关该同位素的说法正确的是( )| A. | 质子数为67 | B. | 电子数为99 | C. | 中子数为67 | D. | 质量数为67 |
分析 根据在原子中,原子序数=核电荷数=质子数=核外电子数,相对原子质量=质子数+中子数,进行解答本题.
解答 解:A.67166Ho的质子数为67,故A正确;
B.16667Ho,因为质子数=核外电子数=67,即电子数为67,故B错误;
C.67166Ho的质子数为67,质量数为166,则该同位素原子核内的中子数为166-67=99,故C错误;
D.67166Ho的质子数为67,质量数为166,故D错误.
故选A.
点评 本题考查原子的构成及原子中的数量关系,明确原子序数=核电荷数=质子数=核外电子数即可解答,题目较简单.

练习册系列答案
相关题目
20.下列5种有机化合物中,能够发生酯化、加成和氧化3种反应的是( )
①CH2=CHCOOH
②CH2=CHOOCH3
③CH2=CHCH2OH
④CH3CH2CH2OH
⑤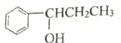
①CH2=CHCOOH
②CH2=CHOOCH3
③CH2=CHCH2OH
④CH3CH2CH2OH
⑤
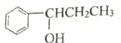
| A. | ①③④ | B. | ②④⑤ | C. | ①③⑤ | D. | ①②⑤ |
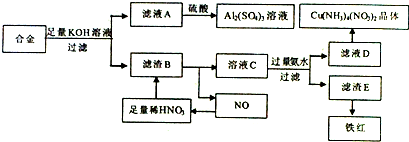
1.现有下列十种物质:①H2②Cu ③Na2O ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧碘酒 ⑨稀硝酸 ⑩Al2(SO4)3
(1)按物质的分类方法填写表格的空白处(填写序号):1⑦⑧⑨;2③④;3③⑤⑥⑩;
(2)⑩在水中的电离方程式为Al2(SO4)3=2Al3++3SO42-;
(3)写出下列物质之间反应的离子方程式:少量的④通入⑥的水溶液CO2+Ba2++2OH-═BaSO4↓+H2O;⑤的水溶液与⑥的水溶液混合2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;
(4)质量都是10g的HCl、NH3、CO2、H2四种气体在标准状况下,体积最小的是CO2,密度最小的是H2;(填分子式)
(5)②与⑨发生反应的化学方程式为:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,HNO3是氧化剂,Cu元素被氧化,参加反应的HNO3中,n(HNO3)被还原:n(HNO3)未被还原=1:3,当有6.4gCu发生反应时,转移电子的物质的量为0.2mol.
(1)按物质的分类方法填写表格的空白处(填写序号):1⑦⑧⑨;2③④;3③⑤⑥⑩;
| 分类标准 | 混合物 | 氧化物 | 电解质 |
| 属于该类的物质 | 1 | 2 | 3 |
(3)写出下列物质之间反应的离子方程式:少量的④通入⑥的水溶液CO2+Ba2++2OH-═BaSO4↓+H2O;⑤的水溶液与⑥的水溶液混合2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;
(4)质量都是10g的HCl、NH3、CO2、H2四种气体在标准状况下,体积最小的是CO2,密度最小的是H2;(填分子式)
(5)②与⑨发生反应的化学方程式为:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,HNO3是氧化剂,Cu元素被氧化,参加反应的HNO3中,n(HNO3)被还原:n(HNO3)未被还原=1:3,当有6.4gCu发生反应时,转移电子的物质的量为0.2mol.
18.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 22.4L氯气中所含分子数为NA | |
| B. | 标准状况下2.24LH2O所含原子数为0.3NA | |
| C. | 1L1mol/LFeCl3溶液所含Cl-数目为NA | |
| D. | 一定条件下1molH2和1molCl2充分反应后生成HCl分子数为2NA |
5.现有如下各化合物:①酒精,②氯化铵,③氢氧化钡,④氨水,⑤蔗糖,⑥高氯酸,⑦氢硫酸,⑧硫酸氢钾,⑨磷酸,⑩硫酸,属于强电解质的是( )
| A. | ②③⑥⑨⑩ | B. | ②③⑥⑧⑩ | C. | ⑥⑦⑧⑨⑩ | D. | ②③④⑥⑧⑨⑩ |
15.在烧杯中加入CuSO4溶液和苯(密度为0.88g/cm3,不溶于水且不与钠反应)各50mL,将一小粒金属钠(密度为0.97g/cm3)投入烧杯中.观察到的现象不可能是( )
| A. | 钠在水层中反应并四处游动 | |
| B. | 钠在苯与CuSO4溶液的界面处反应并作上下跳动 | |
| C. | 烧杯中有气泡产生 | |
| D. | 烧杯底部有蓝色沉淀物 |
2.根据下列三个反应,判断物质的氧化性由强到弱的顺序正确的是( )
①2Fe3++2I-=2Fe2++I2 ②2Fe2++Cl2=2Fe3++2Cl-
③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O.
①2Fe3++2I-=2Fe2++I2 ②2Fe2++Cl2=2Fe3++2Cl-
③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O.
| A. | Fe3+>C12>MnO4- | B. | MnO4->Cl2>Fe3+ | C. | Fe3+>Cl2>I2 | D. | I2>Cl2>Fe3+ |
19.下列实验操作均要用到玻璃棒,其中玻璃棒的作用相同的是①过滤 ②蒸发 ③溶解 ④浓硫酸的稀释( )
| A. | ①和② | B. | ①和③ | C. | ②和③ | D. | ②和④ |