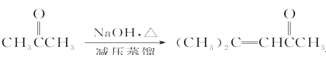题目内容
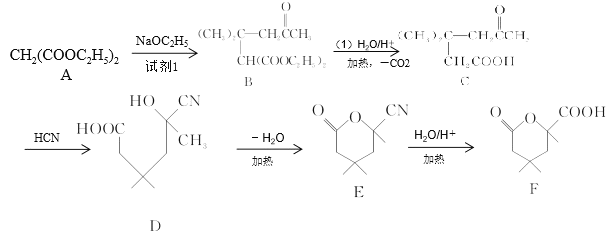
【题目】对羟基苯甲酸丁酯(俗称尼泊金丁酯)可用作防腐剂,对酵母和霉菌有很强的抑制作用,工业上常用对羟基苯甲酸与丁醇在浓硫酸催化下进行酯化反应而制得,以下是某课题组开发的从廉价、易得的化工原料出发制备对羟基苯甲酸丁酯的合成路线:
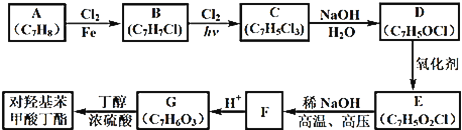
已知以下信息:①通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基;②D可与银氨溶液反应生成银镜;③F的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积比为1﹕1。回答下列问题:
(1)A的化学名称为__;
(2)由B生成C的化学反应方程式为__,该反应的类型为__;
(3)D的结构简式为__;
(4)F的分子式为__;
(5)G的结构简式为__;
(6)E的同分异构体中含有苯环且能发生银镜反应的共有__种,其中核磁共振氢谱有三种不同化学环境的氢,且峰面积比为2﹕2﹕1的是____________(写结构简式)。
【答案】甲苯 ![]() +2Cl2
+2Cl2![]()
![]() 2HCl 取代反应
2HCl 取代反应  C7H4O3Na2
C7H4O3Na2  13
13 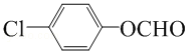
【解析】
由A的分子式为C7H8,最终合成对羟基苯甲酸丁酯可知,A为甲苯![]() ,甲苯在铁作催化剂条件下,苯环甲基对位上的H原子与氯气发生取代反应生成B,B为
,甲苯在铁作催化剂条件下,苯环甲基对位上的H原子与氯气发生取代反应生成B,B为![]() ,结合信息②可知,D中含有醛基,B在光照条件下,甲基上的H原子与氯气发生取代反应生成C,C为
,结合信息②可知,D中含有醛基,B在光照条件下,甲基上的H原子与氯气发生取代反应生成C,C为![]() ,C在氢氧化钠水溶液中,甲基上的氯原子发生取代反应,生成D,结合信息①可知,D为
,C在氢氧化钠水溶液中,甲基上的氯原子发生取代反应,生成D,结合信息①可知,D为![]() ,D在催化剂条件下醛基被氧化生成E,E为
,D在催化剂条件下醛基被氧化生成E,E为![]() ,在碱性高温高压条件下,结合信息③可知,苯环上的Cl原子被取代生成F,同时发生酯化反应,F为
,在碱性高温高压条件下,结合信息③可知,苯环上的Cl原子被取代生成F,同时发生酯化反应,F为![]() ,F酸化生成对羟基苯甲酸G
,F酸化生成对羟基苯甲酸G![]() 。
。
(1)由以上分析可知A的化学名称为甲苯;
(2)B为![]() ,与氯气在光照条件下发生取代反应生成
,与氯气在光照条件下发生取代反应生成![]() ,方程式为
,方程式为![]() +2Cl2
+2Cl2![]()
![]() 2HCl;
2HCl;
(3)由以上分析可知D为 ;
;
(4)F为![]() ,分子式为C7H4O3Na2;
,分子式为C7H4O3Na2;
(5)由元素分析可知F为 ;
;
(6)同分异构体有两种形式,一种是苯环上含有一个酯键和一个氯原子(邻、间、对)共3种异构;另一种是有一个醛基、一个羟基和一个氯原子,这3种不同的取代基共有10种同分异构体,所以共计是13种.其中核磁共振氢谱有三种不同化学环境的氢,且峰面积比为2:2:1的是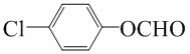 。
。

【题目】四种短周期元素的性质或结构信息如下表所示。请根据信息回答下列问题。
元素 | T | X | Y | Z |
性质或结构信息 | 原子核外s能级上的电子总数等于p能级上的电子总数;人体内含量最多的元素,且其单质是常见的助燃剂 | 其单质为双原子分子,分子中含有3对共用电子对,常温下其气体单质性质稳定,但其原子较活泼 | 其单质质软,是银白色固体,导电性强。单质在空气中燃烧发出黄色火焰 | 第三周期元素的简单离子中半径最小 |
(1)写出元素T的离子结构示意图:______;写出元素X的气态氢化物的分子式:______;写出Z元素原子的核外电子排布式:________;元素Y的原子核外共有_______种形状不同的电子云。
(2)Z单质与Y最高价氧化物的水化物的水溶液反应的离子方程式:______。
(3)元素T与氟元素相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是___(填字母)。
a.常温下氟气的颜色比T单质的深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素显正价
d.比较两元素的单质与氢气化合时得电子的数目