题目内容
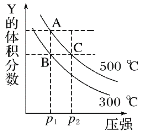
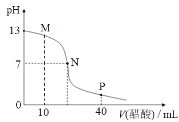
【题目】25℃时,向 20 mL 0.1 mol/L NaOH 溶液中逐滴加入 0.1 mol/L 醋酸溶液,滴定曲线如图所示。下列说法正确的是
A.该NaOH 溶液中水电离出的 c(OH-)=1×10-12 mol/L
B.M 点时,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.P 点时,c(CH3COO-)+c(CH3COOH)=2c(Na+)
D.N 点对应的横坐标是 20
【答案】C
【解析】
A. 0.1 mol/L NaOH 溶液中水电离出的 c(OH-)=1×10-13mol/L,选项A错误;
B.在M点溶液显碱性,根据电荷守恒,则c(Na+)>c(CH3COO-)> c(OH-)>c(H+),选项B错误;
C. P 点时相当于醋酸和醋酸钠按1:1形成的溶液,根据物料守恒有c(CH3COO-)+c(CH3COOH)=2c(Na+),选项C正确;
D. 若N 点对应的横坐标是 20,则醋酸与氢氧化钠恰好反应时,生成的醋酸钠水解,溶液显碱性,与N点溶液显中性不相符,选项D错误。
答案选C。

【题目】表是元素周期表的一部分,请用元素符号、离子符号或相关化学式回答有关问题:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)表中能形成两性氢氧化物的元素在周期表中的位置是________;
(2)写出②的气态氢化物的结构式________;
(3)元素④⑤⑥⑦离子半径由大到小的顺序________;
(4)①、⑥、⑦三种元素的最高价氧化物的水化物中酸性最强的是________;④、⑤、⑨三种元素的最高价氧化物的水化物中碱性最强的是
(5)⑦和⑩氧化性较强的是________用一个置换反应证实这一结论(写化学方程式)___________________________。
(6)④⑤两元素相比较,金属性较强的是________,可以验证该结论的实验是________;
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将形状、大小相同的这两种元素的单质用砂纸打磨后分别和同浓度的盐酸反应
(c)将形状、大小相同两种元素的单质用砂纸打磨后分别和热水作用,并滴入酚酞
(d)比较这两种元素的气态氢化物的稳定性
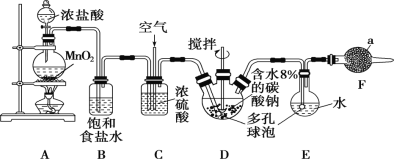
【题目】Cl2O为国际公认的高效安全灭菌消毒剂之一,实验室可利用氯气和空气(氯气与空气体积比为1∶3,空气不参与反应)的混合气与含水8%的碳酸钠反应制备,并用水吸收Cl2O制备次氯酸溶液,所用实验装置和Cl2O的性质如下:
颜色 | 棕黄色 |
状态 | 气体 |
气味 | 强刺激性 |
熔点 | -116 ℃ |
沸点 | 3.8 ℃ |
水溶性 | 极易溶于水,与水反应生成次氯酸 |
热稳定性 | 42 ℃以上分解为Cl2和O2 |
(1)仪器a的名称为________,所盛放的药品是________。
(2)写出装置A中发生反应的离子方程式:_______________。
(3)装置C的主要作用是___________。
(4)装置D、E中都用到多孔球泡,其作用是____________。
(5)写出装置D中Cl2与过量碳酸钠反应生成Cl2O的化学方程式:________。
(6)装置E采用棕色圆底烧瓶的原因是____________。
(7)制备Cl2O装置中存在缺陷,请提出改进措施:___________。