题目内容
【题目】现代社会生活离不开能量。
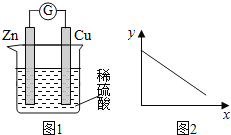
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用______(填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面______(填序号)反应释放的热量加热食物。
A.生石灰和水B.Ba(OH)2·8H2O和NH4Cl
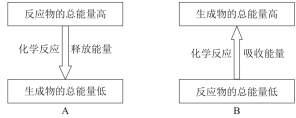
(3)天然气的主要成分是甲烷,它是一种清洁能源。甲烷燃烧是______(填“放热”或“吸热”)反应,其能量变化可用如图中的______(填序号)表示。
【答案】吸热 A 放热 A
【解析】
(1)制作冷敷袋可以利用化学变化或物理变化的吸热降低温度;
(2)即热饭盒应该是利用放热反应放出热量达到升高温度而加热食物目的;
(3)甲烷燃烧是放热反应,放热反应中,反应物的总能量大于生成物的总能量。
(1)制作冷敷袋可以利用化学变化或物理变化的吸热降低温度,达到降温、保鲜和镇痛的目的,故答案为:吸热;
(2)即热饭盒应该是利用放热反应放出热量达到升高温度而加热食物目的,生石灰和水的反应是放热反应,能故达到升高温度的目的,Ba(OH)2·8H2O和NH4Cl的反应为吸热反应,无法达到升高温度的目的,故答案为:A;
(3)甲烷燃烧是放热反应,放热反应中,反应物的总能量大于生成物的总能量,由图可知,图A表示的是反应物总能量大于生成物总能量的放热反应,图B表示的是反应物总能量小于生成物总能量的吸热反应,故答案为:放热;A。

 阅读快车系列答案
阅读快车系列答案【题目】下列实验结论与实验现象相符合的一组是
选项 | 实验 | 现象 | 结论 |
A | 向某盐溶液中加入浓NaOH溶液,加热 | 产生的气体能使湿润的红色石蕊试纸变蓝 | 原溶液中含有 |
B | 把SO2通入紫色的酸性高锰酸钾溶液中 | 溶液紫色褪去 | SO2具有漂白性 |
C | 向蔗糖中滴加浓硫酸 | 蔗糖变黑 | 浓硫酸具有吸水性 |
D | 向盛有Cu片的试管中加入稀H2SO4,无明显现象,再加入NaNO3固体 | Cu片逐渐溶解,产生气 泡,溶液变蓝 | NaNO3是催化剂,可增大Cu与稀H2SO4反应的化学反应速率 |
A.AB.BC.CD.D
【题目】分别向等体积的不含O2、含有O2的0.1mol·L1BaCl2溶液中通入SO2,探究体系中物质间的相互作用,实验记录如下。(已知:pH越小,溶液酸性越强)
pH变化 |
|
溶液中是否产生沉淀 | 不含O2的BaCl2溶液中没有白色沉淀,含有O2的BaCl2溶液中产生白色沉淀。 |
下列说法不正确的是
A.a所示溶液的pH降低的原因:SO2与H2O反应生成H2SO3,溶液的c(H+)增大
B.b所示溶液中发生反应:2Ba2++O2+2SO2+2H2O=2BaSO4↓+4H+
C.b比a所示溶液的pH小的原因:Ba2++SO2+H2O=BaSO3↓+2H+
D.SO2通入不含O2的BaCl2溶液后,再通入NH3,产生BaSO3沉淀