题目内容
【题目】在一定温度下,向2 L恒容密闭容器中充入1 mol A,发生2A(g)![]() B(g)+C(g)反应。反应过程中c(C)随时间变化的曲线如图所示,下列说法不正确的是( )
B(g)+C(g)反应。反应过程中c(C)随时间变化的曲线如图所示,下列说法不正确的是( )
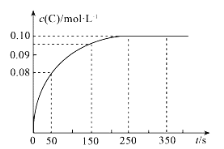
A.反应在0~50 s的平均速率v(C)=1.6×10-3molL-1s-1
B.该温度下,反应的平衡常数K=0.025 molL-1
C.保持其他条件不变,升高温度,平衡时c(B)=0.09 molL-1,则该反应的H<0
D.反应达平衡后,再向容器中充入1 mol A,该温度下再达到平衡时,A的转化率不变
【答案】B
【解析】
A.反应在0~50 s的平均速率v(C)=![]() =1.6×10-3molL-1s-1,A正确;
=1.6×10-3molL-1s-1,A正确;
B.该温度下,平衡时,c(C)=0.10mol/L,则c(B)=0.10mol/L,c(A)= 0.50mol/L-0.20mol/L=0.30mol/L,反应的平衡常数K=![]() ≈0.11 molL-1,B不正确;
≈0.11 molL-1,B不正确;
C.升高温度,平衡时c(B)=0.09 molL-1<0.10 molL-1,则平衡逆向移动,该反应的H<0,C正确;
D.反应达平衡后,再向容器中充入1 mol A,相当于加压,平衡不发生移动,A的转化率不变,D正确;
故选B。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
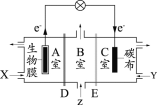
同步拓展阅读系列答案【题目】为研究铁盐与亚硫酸盐之间的反应,某研究小组利用孔穴板进行了实验探究:

小组记最的实验现象如下表所示:
开始时 | 5min 后 | 3天后 | |
实验I | 溶液立即变为红褐色,比II、III中略浅 | 与开始混合时一致 | 溶液呈黄色,底部出现红褐色沉淀 |
实验II | 溶液立即变为红褐色 | 红褐色明显变浅 | 溶液呈黄绿色 |
实验III | 溶液立即变为红褐色 | 红褐色变浅,比II中深 | 溶液呈黄色 |
(1)测得实验所用0.4mol/LFeCl3溶液及Fe(NO3)3溶液pH均约为1.0。两溶液均呈酸性的原因是_______________(用离子方程式表示)。
(2)开始混合时,实验I中红褐色比II、III中略浅的原因是____________________________。
(3)为了探究5min后实验II、III中溶液红褐色变浅的原因,小组同学设计了实验IV;分别取少量 5min后实验I、II、III中溶液,加入2滴铁氰化钾溶液,发现实验II、III中出现蓝色沉淀,实验I中无明显变化。试用方程式解释溶液中出现Fe2+的原因______________________________。
(4)针对5min后实验III中溶液颜色比实验II中深,小组同学认为可能存在三种因素:
①Cl-可以加快Fe3+与SO32-的氧化还原反应:
②NO3-可以______________________________;
③NO3-在酸性环境下代替Fe3+氧化了SO32-,同时消耗H+,使Fe3+水解出的Fe(OH)3较多。
通过实验V和实验VI进行因素探究:
实验操作(己知Na+对实验无影响) | 5min后的现象 | |
实验V | 在2mLpH=1.0的0.4mol/L Fe(NO3)3溶液中溶解 固体,再加入2滴0.4mol/L Na2SO3溶液 | 溶液的红褐色介于II、III之间 |
实验VI | 在2mLpH=1.0的稀硝酸中溶解约0.19gNaNO3固体,再加 入2滴0.4mol/LNa2SO3溶液。向其中滴入少量BaCl2溶液 | _______________________。 |
实验结论:因素①和因素②均成立,因素③不明显。请将上述方案填写完整。
(5)通过上述时间,以下结果或推论合理的是_______________(填字母)。
a.Fe3+与SO32-同时发生水解反应和氧化还原反应,且水解反应的速率快,等待足够长时间后,将以氧化还原反应为主
b.浓度为1.2mol/L的稀硝酸在5min内不能将Fe2+氧化
c.向pH大于1的稀硝酸中加入少量Ba(NO3)2,使其完全溶解,可用来检验实验1的上层淸液中是否存在SO42-