��Ŀ����
����Ŀ��Cl2���仯�����������������о��й㷺����;������������ˮ���γ���������ˮ��ϵ��
���������գ�
��1����ԭ���������ӵĵ����Ų�ʽ��__��������Ų�ʽ��ȣ������ʾʽ�����˶Ժ�������˶�״̬��__������
��2���⡢�ȡ�������Ԫ�ظ����γ�һ�ּ������ӣ������Ӱ뾶�ɴ�С��˳��������Щ����__��
��3����������ˮ��ϵ�У����ڶ������Ԫ�ص�ƽ���ϵ����ֱ���ƽ�ⷽ��ʽ��ʾ��__����֪HClO��ɱ��������ClO��ǿ���ȴ�������ˮʱ�����ļ���ɱ��Ч�����ڶ��������ԭ����__��һ��ԭ�ɣ���
��4������ˮ�У����й�ϵ��ȷ����__��ѡ���ţ���
a c��HClO��+c��ClO����=c��H+����c��OH����
b c��H+��=c��ClO����+c��Cl����+c��OH����
c c��HClO����c��Cl����
d c��Cl������c��OH����
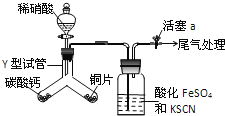
��5��ClO2��һ�ָ���Ч����ȫ������������ҵ�Ͽ���ClO2��ˮ�е�MnCl2�ڳ����·�Ӧ������MnO2�����ᣬ�Գ�ȥˮ��Mn2+��д���÷�Ӧ�Ļ�ѧ����ʽ������ƽ��__��������Ϊ����MnO2������������Ӧ����������������ʶ����__����������������������˵������__��
���𰸡�3s23p5 �������� Cl����O2����H�� Cl2��aq��+H2O![]() HClO+H++Cl����HClO
HClO+H++Cl����HClO![]() H++ClO����Cl2��g��
H++ClO����Cl2��g��![]() Cl2��aq�� �ļ��¶ȸߣ�HClO�ֽ⣬ɱ��Ч�����ڶ����� bc 2ClO2+5MnCl2+6H2O=5MnO2+12HCl �� MnO2��Ũ������ȵ������²��ܷ�Ӧ
Cl2��aq�� �ļ��¶ȸߣ�HClO�ֽ⣬ɱ��Ч�����ڶ����� bc 2ClO2+5MnCl2+6H2O=5MnO2+12HCl �� MnO2��Ũ������ȵ������²��ܷ�Ӧ
��������
��1������17��Ԫ�أ����������ӵĵ����Ų�ʽΪ![]() �����ù����ʾʽ���������������������ӵ���������
�����ù����ʾʽ���������������������ӵ���������
��2��![]() �൱�ڹ�ͺͺ�����ӣ�
�൱�ڹ�ͺͺ�����ӣ�![]() ������ǰ������ӣ���
������ǰ������ӣ���![]() ������ǰ������ӣ��뾶�ɴ�СΪ
������ǰ������ӣ��뾶�ɴ�СΪ![]() ��
��
��3���������������ܽ⡪�ӷ�ƽ�⣬��![]() ������������ܺ�ˮ�������淴Ӧ����
������������ܺ�ˮ�������淴Ӧ����![]() ����
����![]() ��һ�����ᣬ���ڵ���ƽ��
��һ�����ᣬ���ڵ���ƽ��![]() �� �ļ��Ͷ��������������¶ȣ�����֪��
�� �ļ��Ͷ��������������¶ȣ�����֪��![]() �����ֽ⣬���ɱ��Ч����
�����ֽ⣬���ɱ��Ч����
��4��a.��Һ�д��������غ�![]() ����Ҫa���������
����Ҫa���������![]() �����Ƕ��߲�������ȣ�a�����
�����Ƕ��߲�������ȣ�a�����
b.�����Һ�д��ڵ������غ㣬b����ȷ��
c.������ˮ��Ӧ�õ�������![]() ��
��![]() ��
��![]() ��ǿ�������ȫ���룬�����Һ��
��ǿ�������ȫ���룬�����Һ��![]() �����������ɵ�
�����������ɵ�![]() ��������
��������![]() ��������ʲ��ֵ��룬���ʣ���
��������ʲ��ֵ��룬���ʣ���![]() ��Ũ�Ƚ�С��
��Ũ�Ƚ�С��![]() ��Ũ�ȣ�c����ȷ��
��Ũ�ȣ�c����ȷ��
d.��ˮ�����ԣ������Һ�е�![]() ���ͣ�������
���ͣ�������![]() ������˲����ܳ���
������˲����ܳ���![]() �������d�����
�������d�����
��ѡbc��
��5��![]() ����������
����������![]() ����ԭ�������߷���������ԭ��Ӧ
����ԭ�������߷���������ԭ��Ӧ![]() ���÷�Ӧ�õ��������ϡ����û�м��ȣ���˲�̫���ܱ�
���÷�Ӧ�õ��������ϡ����û�м��ȣ���˲�̫���ܱ�![]() �������������������Ӧ����һ����ֹͣ�ˡ�
�������������������Ӧ����һ����ֹͣ�ˡ�

 ��У����ϵ�д�
��У����ϵ�д�